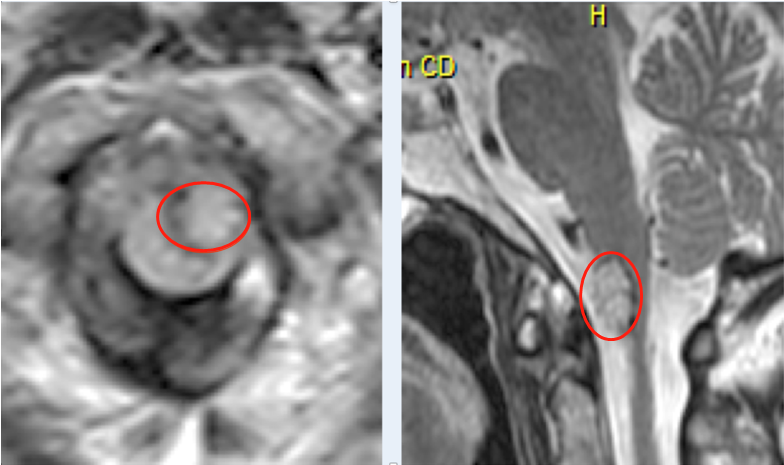
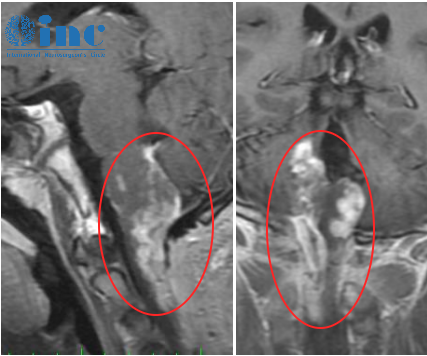
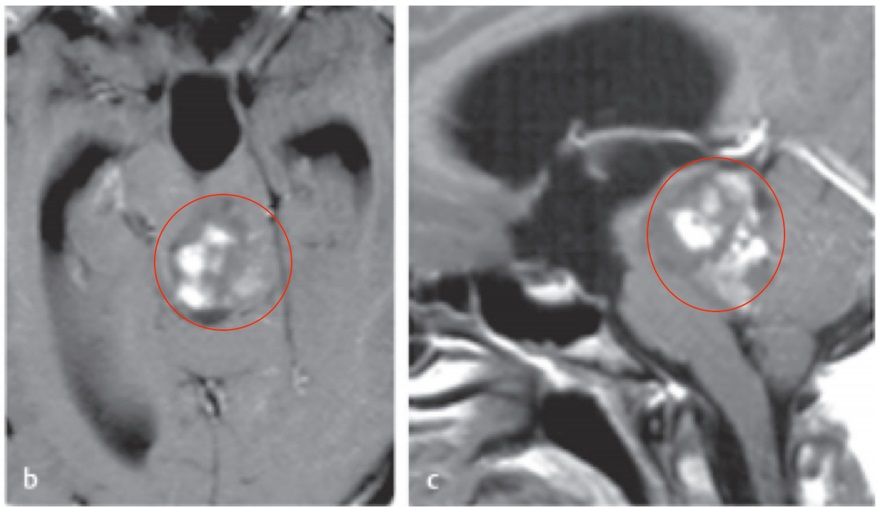
STAT3与脑胶质瘤的关系,STAT3同样是STATs家族成员之一,其编码基因位于17号染色体上,较初因其在IL-6(interleukin-6)介导的炎症反应中能够转录一组靶基因而被关注。

STAT3蛋白大约由770个氨基酸组成,有STAT3α、STAT3β、STAT3γ和STAT3δ四种变异体,STAT3α是STAT3主要存在形式,有705位的酪氨酸磷酸化位点和727位的丝氨酸磷酸化位点,普遍认为STAT3信号传导通路与细胞的增殖、分化及凋亡密切相关,该通路持续激活可导致细胞异常增殖和恶性转化,目前被定义为癌基因。国内张煜等发现STAT3在胶质瘤中广泛表达,而在瘤周组织及正常组织中的表达通常较低或不表达。
研究表明,许多肿瘤组织包括胶质瘤、肝癌及腺癌细胞中STAT3及其下游基因,如细胞周期蛋白D1(cyclinD1)、c-Myc、Bcl-2、Bcl-xl和VEGF等,常显示异常表达或活性增强,从而使细胞生长失控,控制肿瘤细胞的凋亡,促进肿瘤细胞的增殖,诱导肿瘤血管生成,参与肿瘤免疫逃逸,控制免疫功能,较终导致恶性肿瘤的发生和发展。
1促进存活和增殖作用
许多研究表明控制STAT3途径可导致抗凋亡基因产物如Survivin、Bcl-xl、Bcl-2和Mcl-1低表达,并且细胞周期调节物如c-Myc、cyclinD1和cyclinE同样低表达。通过控制细胞周期和细胞凋亡的调节剂,控制STAT3活性后肿瘤细胞死亡增加,这些充分解释了STAT3控制肿瘤细胞凋亡,促进肿瘤细胞的增殖功能。
较近的证据一致认为STAT3的生物学功能归因于除Y705酪氨酸磷酸化之外的翻译后修饰,包括赖氨酸甲基化和乙酰化以及727位点丝氨酸磷酸化(pSTAT3-S727),主要为pSTAT3-S727,由于STAT3活性已通过靶向pSTAT3-Y705或基因沉默或STAT3二聚体形成被调节,对pSTAT3-S727在STAT3调节细胞方面的研究尚不充分。S727磷酸化是通过蛋白激酶C(PKC)家族成员的丝氨酸/苏氨酸激酶如PKC-ε调节,同时MAP激酶途径下游的其他激酶也被报道参与STAT3-S727磷酸化,并且较近表明pSTAT3-S727的生物学功能和调控取决于细胞类型和细胞分化状态。
综合考虑目前的数据,很明显STAT3在许多细胞过程的控制中起关键作用,然而,pSTAT3-Y705和pSTAT3-S727在这些过程中的贡献仍不清楚,根据目前知识,可以推测一些基因只被pSTAT3-Y705和pSTAT3-S727中的一个或两个所优先调节,在涉及磷酸化的情况下,它们的作用可以是一致或不一致的。Xu等发现敲除PKCε后pSTAT3-S727和Bcl-xl的表达减弱,但另一个STAT3下游靶标的Bcl-2的表达无明显减弱,作者推测敲低PKCε可能影响通过互相补偿调节Bcl-2表达的信号通路,也有学者推测,因为敲低PKCε不会影响pSTAT3-Y705,所以它可能维持了Bcl-2的表达,当然以上推测都有待于进一步验证。
据报道microRNA-506(miR-506)和microRNA-519a(miR-519a)可作为肿瘤控制剂,通过靶向STAT3mRNA并降低STAT3靶基因的表达来控制神经胶质瘤细胞增殖。
综上,STAT3主要通过pSTAT3-Y705和pSTAT3-S727这两种激活方式促进肿瘤细胞的存活和增殖。
2迁移和侵袭作用
JAK/STAT3活化是胶质瘤进展和侵袭的重要因素,即STAT3信号直接调节MMP-2和9的表达,进而促进肿瘤侵袭和转移。国外学者Cho等在研究壳二孢对胶质瘤迁移和侵袭时发现壳二孢控制JAK2和STAT3磷酸化、STAT3DNA结合活性的核易位进而控制癌细胞迁移和侵袭,该研究充分证实了STAT3在胶质瘤迁移和侵袭中的重要作用,在较近的一项肝癌细胞的研究中显示,通过控制STAT3信号,同样控制了肝癌细胞的侵袭和生长。
3免疫逃避作用
研究发现活化的STAT3可通过干扰自身和适应性免疫系统来促进癌细胞逃避免疫监视。肿瘤细胞通过质膜相互作用和释放细胞因子如IL-6、8、10和PGE-2腺素,激活STAT3诱导胶质瘤细胞逃避免疫监视。也有报道,胶质瘤细胞中激活STAT3可阻断树突细胞的分化、成熟功能,控制T细胞增殖,此外,较近一项研究表明胶质瘤干细胞通过IL-6、10激活STAT3信号通路,进而激活肿瘤巨噬细胞中B7-H4表达,B7-H4在肿瘤微环境中围绕基质和侵入边缘可能通过阻断T细胞功能诱发肿瘤细胞逃避免疫监视。
另外,也有研究报道缺氧也可引起神经胶质瘤诱导的免疫控制,且可能被STAT3控制剂阻碍或逆转,表明使用STAT3控制剂在胶质瘤免疫治疗中的可能性。然而,控制STAT3并不能阻止IL-6诱导的朗汉斯细胞分化免疫控制,就表明STAT3激活不是胶质瘤诱导的免疫耐受的机制,因此,有学者提出STAT3和p38MAPK途径的联合控制作为协同抗癌免疫治疗方法。
4血管生成作用
在U87MG中发现通过pSTAT3-Y705激活STAT3后VEGF高表达,而敲除STAT3基因后,见肿瘤细胞生长缓慢甚至凋亡,提示STAT3通过VEGF调控胶质瘤血管生成。同时,胶质瘤中血管生成伴随VEGF-A诱导的内皮细胞中钙蛋白酶控制剂(CAST)下调,CAST的下调触发μ-钙蛋白酶诱导SOCS3蛋白水解和随后刺激VEGF-C转录的STAT3超活化,诱导的VEGF-C和VEGF-A在血管生成中起到协同作用。因此,将STAT3的调节整合到抗血管生成治疗策略中可能有意义,因为它的作用,至少部分是作为上游调节因子,不仅与血管生成有关,还与自噬和缺氧诱导的生物效应有关。国外已用抗VEGF单克隆抗体贝伐单抗以及VEGFR的化学控制剂用于治疗复发的脑胶质瘤患者,但是在顺利性和生存期延长方面没有达到预期目标。
- 文章标题:STAT3与脑胶质瘤的关系
- 更新时间:2021-11-11 14:50:00

 400-029-0925
400-029-0925