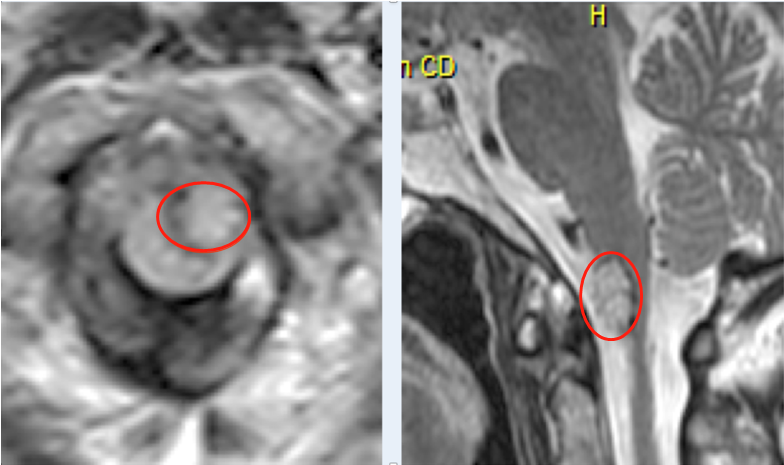
脑胶质瘤是成人中较常见的原发性颅内恶性肿瘤。即使经过深入的多学科治疗,其特征仍然是复发。它们表现出广泛的渗透性生长行为,但很少转移到远处的器官。侵袭性生长模式是神经胶质瘤较突出的特征,也是肿瘤复发的主要原因之一。即使是低度脑胶质瘤也是渗透性的,更不用说恶性神经胶质瘤了。对局部复发风险高的患者的研究可能会为分子靶向治疗提供更多的线索。
肿瘤的大小、增殖指数和肿瘤水平与局部复发的发生密切相关。然而,为了进一步结合分子靶向治疗,仍迫切需要揭示与局部复发发展相关的新生物因素。
通过研究细胞外基质、细胞粘附分子和蛋白酶的关键作用,确定了肿瘤入侵的主要过程。几项研究表明,基质金属蛋白酶在神经胶质瘤入侵机制中起着关键作用。MMP锌依赖蛋白水解酶参与细胞外基质的重塑和降解。研究还发现,MMP生理和病理过程可以通过裂解细胞因子、趋化因子和生长因子来调节。
作为23种与结构相关的酶之一,它们分为明胶酶、间质胶原酶和广泛的特异性基质溶菌素。根据其基质亲和力和其他变体。MMP各种肿瘤,包括乳腺肿瘤调查。恶性肿瘤患者血清MMP-2和MMP-水平上升,并与不良预后成正有关。
积累的证据表明,MMP-2促进血脑屏障、神经变性过程和血管生成降解。然而,血清MMP-9级似乎更相关,健康个体在生理条件下几乎无法检测到MMP-9。一旦MMP它被一组内源性控制剂控制。TIMP-1与PRO-MMP-9特异性相互作用,TIMP-2优先与PRO-MMP-2结合。从理论上讲,TIMP-1/2可预防肿瘤生长、局部浸润和转移。
关于TIMPS对癌症进展功能的较新研究引起了很大的争议。TIMP-表达式的增加可以促进癌细胞的增殖和入侵,并已证明在某些肿瘤中,TIMP-表达的增加与癌症的进展和不良预后有关。MMP和TIMP血管生成、组织重塑和修复过程中的动态平衡ECM重塑起着基本作用。MMP-2和MMP-9增强了黑色素瘤的入侵和血源性转移,但MMP-2与黑色素瘤患者的不良生存有关。

肿瘤复发时经常测试分子靶向疗法。大多数分子数据来自较初的肿瘤。为了进一步结合分子靶向治疗,仍迫切需要揭示基质金属蛋白酶在原发性和复发性肿瘤中的表达差异及其对生存的影响。本研究旨在检测原发性神经胶质瘤和复发性神经胶质瘤MMPS和TIMPS表达差异。虽然许多研究已经探索了神经胶质瘤复发的机制,并证明了几种生物分子与神经胶质瘤复发有关,可以帮助识别高危患者和神经胶质瘤预后因素分子标记仍难以捉摸,迫切需要识别分子预后标记可以独自评估患者的生存。
观察胶质瘤观察原发和复发胶质瘤MMP-9,MMP-2,TIMP-1和TIMP-表达2,分析其与临床病理特征的关系。此外,到它们的预后意义。胶质瘤细胞U本研究采用251和原位异种移植模型。
该研究包括100名神经胶质瘤患者。将手术与疾病复发之间的时间定义为无病间隔。从原发诊断的手术时间到死亡或较终随访日期,计算原发肿瘤的总生存期。年龄、性别、辅助放疗、组织学等级、肿瘤位置、DFI和OS状态。平均年龄为40.89岁。DFI和OS平均时间为33.04个月和56.11个月。复发性脑胶质瘤水平与原发性脑胶质瘤水平明显不同,表明复发后原发性神经胶质瘤恶性程度增加。
在57例高级原发性神经胶质瘤患者中,复发时只有2例变为低级。这100例患者中MMP-2,MMP-9,TIMP-1和TIMP-2的蛋白质表达。在这些复发性肿瘤组织中,蛋白质表达的变化很多。它评估了每种蛋白质的免疫反应。无一抗的免疫组织化学作为对照染色。血管内皮细胞生物标记物MMP-2,-9和CD31进行了双重染色,结果MMP-2,-9和CD31的共同定位较少,说明MMP-2和MMP-9主要位于肿瘤细胞中,但也位于基质细胞中。
每种蛋白质表达的免疫反应评分在原发性组织和复发性组织之间存在差异。卡方检验显示,MMP-2和MMP-9表达阳性复发性胶质瘤的百分比明显高于初级胶质瘤。MMP-原发性疾病与复发性疾病的不一致率为46%。在MMP-85个表示阴性的原发组织中,44个在复发组织中呈阳性。MMP-原发性和复发性疾病之间的不一致率为42.0%。随着肿瘤的复发,TIMP-1和TIMP-2阳性病例的百分比降低。
在34例患者中发现TIMP-1不一致。原发组织28例TIMP-表达阳性,复发时阴性。相比之下,63例患者中只有6例处于手术一阶段TIMP-1表达阴性,在复发阶段,TIMP-1表达阳性。同样,TIMP-2的表达也不同。
原发性肿瘤和复发性肿瘤MMP-9的表达与肿瘤分级呈正相关。原发性肿瘤和复发性肿瘤。另一方面,在原发性和复发性肿瘤中,TIMP-2表达与肿瘤分级无相关性。TIMP-1与原发性肿瘤分级呈正相关,与复发性肿瘤无正相关。MMP-2和MMP-同时,阳性表达在高度恶性肿瘤中更为常见。为了分析放疗对肿瘤标志物变化的影响,根据全部患者在一开始手术后是否接受放疗,将其分为几组。
年龄、性别、组织学等级、位置、DFI,OS,MMP2和TIMP-1/2的差异没有统计意义。两组之间MMP-9的表达差异。二进制逻辑分析表明,放疗后,MMP-9明显增加。癌细胞辐射后MMP-9的增加。KAPLAN-MEIER估计揭示DFI与年龄、肿瘤分级、MMP阳性表达与明显不同。通过相关分析,DFI年龄、肿瘤等级,但不是MMP-9。多变量COX分析显示,老年人和高肿瘤的分类是DFI独自预后因素。
但是MMP-2和MMP-9不是DFI独自因素。OS与年龄呈负相关,等级,MMP-2,但不是TIMP-1或TIMP-2。
神经胶质瘤细胞系U251细胞中MMP-9的表达。QRT-PCR结果表明,辐射处理后,MMP-9的表达增加。然后尝试使用脑神经胶质瘤模型来测试辐射在体内是否有相同的效果。与阴性对照组相比,放射治疗组中的免疫组织化学结果MMP-9的表达要高得多。凝胶酶照相法用于测试蛋白酶的水平。结果表明,辐射在胶质瘤细胞的条件培养基和体内胶质瘤提取物中会诱导更多的活性MMP-9.脑神经胶质瘤模型。
导致脑神经胶质瘤模型。MMP-9照射时的分泌增加之一是NF-ΚBP65.在研究中进行了免疫荧光分析,以发现其潜在机制,辐射处理后,NF-ΚBP65易位到U这支持了251细胞的结果。但是,需要更多的实验。全部这些数据表明,辐射增加MMP-9的表达。
以上就是“胶质瘤复发预后怎么样?”的全部内容,想要了解更多“胶质瘤预后”相关问题请咨询我们,INC一直致力加强疑难病症救治、助患者享医疗水平、追求神经外科医术之好,需者可电话400-029-0925详细垂询学术交流、远程咨询、联合咨询或教授主刀等水平服务。
- 文章标题:胶质瘤复发预后怎么样?
- 更新时间:2022-11-24 11:19:09

 400-029-0925
400-029-0925