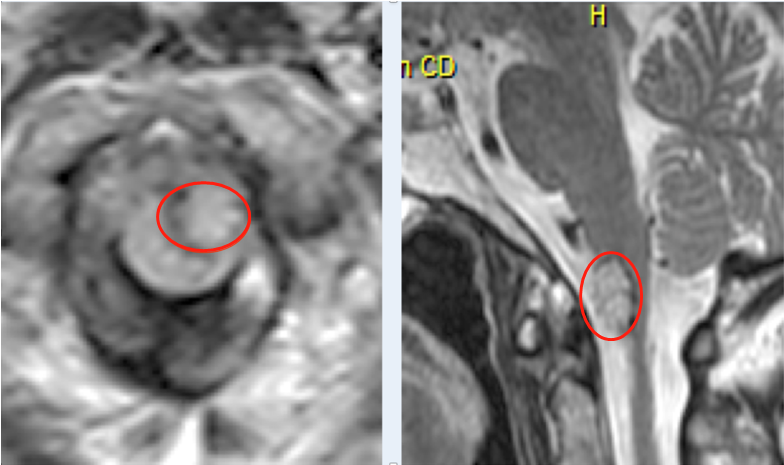
脑胶质瘤是中枢神经系统中较常见的恶性肿瘤。胶质瘤的进展与复杂的基因相互作用和分子调节网络有关。积累的研究重点是寻找分子调节网络,探索可靠的诊断标志物和合适的治疗目标。越来越多的长非编码RNA成为肿瘤起源和进展的新调节剂。LNCRNAS不同类型肿瘤的恶性行为,包括异常表达水平紧密相连的恶性行为,包括GBM。
例如,LNCRNATSLC1-AS1是神经胶质瘤中的一种新型肿瘤控制因子。CRNDE作为一种长期的非编码RNA,通过调节MTOR信号传导增强了神经胶质瘤细胞的生长和入侵。LNCRNAEGFR-AS1是EGFR反义转录物在调节胃癌、肝细胞癌、肾细胞癌等各种肿瘤生长中起着关键作用。
EGFR-AS对神经胶质瘤进展的影响尚不清楚。MIRNA可与靶基因结合MRNA的3'-UTR,导致MRNA降解或翻译过程控制。MIRNA调节肿瘤恶性程度的作用。很少有人报道哪一个MIRNA可能是EGFR-AS1可能冥想癌症进程的目标,包括胶质瘤。
在本研究中,研究人员检查EGFR-AS1在神经胶质瘤发展中的作用。它显示在胶质瘤细胞系和组织中EGFR-AS1表达提高。功能分析表明,EGFR-AS控制神经胶质瘤的进展。EGFR-AS1充当MIR-133B海绵,而MIR-133B可以靶向RACK1的3'-UTR。总的来说,本研究的重点是探索EGFR-AS神经胶质瘤发展中的一轴机制。
RT-QPCR分析表明,与人类正常星形胶质细胞相比,人类胶质瘤细胞系中的胶质瘤细胞EGFR-AS1表达明显上调。表明与NT与人神经胶质瘤组织相比,EGFR-AS1表达增加。进一步探索EGFR-AS1在神经胶质瘤细胞中的作用构建了稳定性EGFR-AS沉默的细胞。EGFR-AS1击倒CCK8和分析的EDU减少神经胶质瘤细胞中的细胞增殖。独自于锚固的生长分析证实了EGFR-AS1基因降低在控制神经胶质瘤细胞增殖中的作用。
与SICTRL组相比,EGFR-AS1敲低减少了胶质瘤细胞的迁移和侵袭。U87和U251细胞中的EGFR-AS1敲低诱导细胞凋亡。蛋白质痕迹分析表明EGFR-AS1的减少导致与转移相关的信号表达下降。EGFR-AS1.降低能高度诱导凋亡分子的表达,包括BAX,裂解的CASPASE-3和PARP。在BCL-表达的变化被称为临界抗凋亡信号中检测到的相反结果。
EGFR通常在肿瘤发生中起到致癌作用。EGFR-AS1转录上EGFR反义链和有EGFR部分序列互补。发现在EGFR-AS1敲低的U87和U251细胞中,EGFRMRNA蛋白质表达水平降低。免疫荧光分析得到证实EGFR-AS神经胶质瘤细胞中的基因降低1EGFR的减少。这些结果表明EGFR-AS1可以调节EGFR表达控制神经胶质瘤的进展。

与AST与人神经胶质瘤细胞系相比,MIR-133B表达水平明显下降。在人神经胶质瘤组织样品中检测到MIR-133B减少表达。进一步探索MIR-133B神经胶质瘤细胞的作用,将AGOMIR-133B和ANTAGOMIR-133B分别转染给人U87和U251细胞分别表达和控制MIR-133的表达。MIR-133B表达控制C–E,U87和U251细胞的细胞增殖和生长活力,MIR-133B细胞增殖和生长能力较高。
与NC与小组相比,促进MIR133B表达能减少胶质瘤细胞的迁移和侵袭。控制MIR-133B神经胶质瘤细胞的迁移和和侵袭的数量。MIR-133B过度表达导致神经胶质瘤细胞凋亡,MIR-133B控制控制凋亡。此外,过度表达MIR-133B在神经胶质瘤细胞中检测到N-钙粘着蛋白,波形蛋白,MMP-2和BCL-2的表达减少。BAX,裂解CASPASE-3和PARP表达水平明显提高。
这些效应可以通过MIR-133B低来逆转。建议EGFR-AS1敲低上调神经胶质瘤细胞MIR-133B表达。进一步识别分子机制EGFR-AS增殖、迁移、浸润和神经胶质瘤细胞凋亡,EGFR-AS1的靶MIRNA评估使用的计算算法。MIR-133B被评估为EGFR-AS1的靶标。双荧光素酶报告基因测定表明,MIR-133B表达降低了神经胶质瘤细胞中野生型的含量EGFR-AS1报告基因的荧光素酶活性。
与AST组和NT与神经胶质瘤细胞系和组织相比,分别检测到RACK1显着升高。与NT与神经胶质瘤组织相比,RACK蛋白质表达增加,和AST与神经胶质瘤细胞相比,RACK蛋白质表达也增加了。通过胶质瘤细胞的增殖和生长能力RACK1的过度表达好转,而在RACK1敲低细胞受到控制。RACK1的过度表达促进了迁移和入侵,同时控制了迁移和入侵U87和U251细胞凋亡。
但是,这些影响都受到了影响RACK1降低所抵消。在过度表达RACK观察神经胶质瘤细胞1N-钙粘着蛋白,波形蛋白,MMP-2和BCL-2的表达增加。相反,RACK1的过表达使BAX,裂解的CASPASE-3和PARP表达水平降低。这些发现在RACK神经胶质瘤细胞中的基因降低被逆转。促进MIR-133B胶质瘤细胞中的表达减少RACK1的表达,并且具有MIR-133B在控制作用的胶质瘤细胞中检测到相反的结果。
将RACK1评估为MIR-133B目标,并将EGFR-AS1中评估的MIR-133B相互作用的位点MIR-133B降低了U87和U251细胞含有野生型RACK1报告基因的荧光素酶活性,但未能控制突变MIR-133B结合位点的报告基因。
以上就是“神经胶质瘤转移的研究”的全部内容,想要了解更多“胶质瘤转移”相关问题请咨询我们,INC一直致力加强疑难病症救治、助患者享医疗水平、追求神经外科医术之好,需者可电话400-029-0925详细垂询学术交流、远程咨询、联合咨询或教授主刀等水平服务。
- 文章标题:神经胶质瘤转移的研究
- 更新时间:2022-11-24 11:13:25

 400-029-0925
400-029-0925