摘要:详细介绍脑干胶质瘤影像学、病理学、分子学分型
是什么决定着脑干胶质瘤手术、放化疗方案制定及预后评估,跟着专家咨询共识一文深入了解。
脑干胶质瘤(brainstem gliomas,BSG)是一组起源于中脑、脑桥和延髓的胶质瘤总称。20世纪80年代之前BSG曾被认为是一组均质性疾病,由于当时脑干仍然是手术禁区,无法进行手术,导致对BSG的病理学特性缺乏足够的认识,加之肿瘤本身对放疗和化疗不敏感,所以BSG的整体预后较差。近30年来,随着神经影像技术、分子生物学、肿瘤基因组学的不断发展,人们逐渐认识到BSG是一组具有高度异质性的疾病。首先,BSG作为一个整体,与大脑半球胶质瘤具有不同的分子遗传学特性;其次,在BSG中,不同年龄组和不同部位的肿瘤具有不同的发病机制、生长特点以及预后。从手术的角度考虑,尽管近30年来随着显微神经外科手术技术、神经影像技术、神经导航技术和神经电生理技术的发展,BSG的手术顺利性和切除程度已取得了进步,但是脑干仍然是中枢神经系统中手术风险较高的部位。而且脑干内不同部位、不同生长方式的肿瘤在手术方案的选择、手术并发症及围手术期护理方面具有各自的特点。BSG本身的异质性、复杂性决定了它需要多学科参与的综合治疗。目前,国内各医疗单位尚无围绕BSG的多学科研究与治疗团队。另外,医疗技术的地域差异导致了对BSG仍缺乏统一的认识。所以,有必要制订BSG规范咨询的专家共识,供广大医疗机构和医务人员在临床工作中参考应用。
流行病学
BSG的发病高峰年龄呈双峰分布,儿童为5~10岁,成人为30~50岁;BSG约占儿童颅内肿瘤的10%~20%,约占成人颅内肿瘤的2%~4%。男女两性发病率之间的差异无统计学意义。BSG的病因尚不清楚,近几年的相关研究显示,H3F3A、HIST1H3B/C、IDH1、TP53、PPM1D、ACVR1、BRAF等基因突变与BSG发病相关。除此之外,部分BSG患者与1型神经纤维瘤病(neurofibromatosis type 1,NF1)相关。
临床表现
BSG的常见临床表现包括:脑神经功能障碍、长束征和共济失调。脑神经功能障碍是脑神经纤维或核团损伤所导致,可反映肿瘤的部位和累及范围,具有定位诊断价值。长束征是指脑干内长的纵行纤维束受累所表现出的临床征象,主要包括皮质脊髓束损伤导致的对侧肢体痉挛性瘫痪、肌张力增高、腱反射亢进、病理征阳性;脊髓丘脑束损伤导致的对侧肢体粗略触压觉和痛温觉异常;内侧丘系损伤导致的对侧肢体意识性本体感觉和细致触觉异常。共济失调主要为小脑脚损伤所致,内侧丘系损伤可导致感觉性共济失调。BSG常见的临床综合征见表1。肿瘤阻塞脑脊液循环通路后可形成幕上脑积水,出现头痛、呕吐、视盘水肿或视神经萎缩等颅内压增高的表现。

此外,儿童BSG患者常有非典型临床表现,可于患者就诊前数月出现,表现为脾气暴躁、攻击行为(攻击对象主要为父母)、睡梦中大哭或大笑、多汗、大小便困难等。
影像学分型
目前BSG尚无统一的影像学分型标准。从1985年至2000年,有关BSG先后有7~8种分型标准。影像学分型的目的是判断肿瘤是否适合外科治疗,预估手术风险及判断预后。在众多分型方法中,较重要的参考依据是肿瘤的生长方式(外生/内生、局灶/弥散),其次是肿瘤的起源部位。本共识在总结临床实践经验的基础上结合既往的分型标准,提出了中国BSG影像学分型标准,该分型在影像学特点的基础上加入了特定部位、特定类型肿瘤的生物学特性,目的是指导临床治疗方案的选择。
一、根据MRI肿瘤生长特点将BSG分为3型
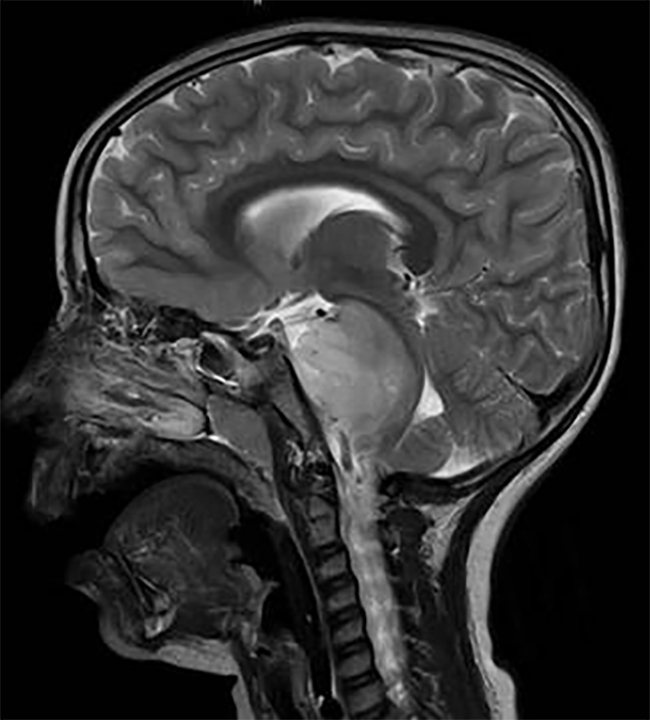
Ⅰ型:外生型BSG,肿瘤向外生长,主体位于脑干外部(图1A)。
Ⅱ型:内生型BSG,可分为Ⅱa型即局灶内生型(图1B)和Ⅱb型即弥散内生型。对Ⅱb型BSG建议行11C-MET PET检查,综合MRI增强扫描的特点和MET摄取情况,可将Ⅱb型肿瘤分为伴有局灶性强化或高代谢的Ⅱb1型(图1 C~E)和无局灶性强化或高代谢的Ⅱb2型(图1F~H)。
Ⅲ型:为不同类型的BSG,Ⅲa型为顶盖胶质瘤(图1I);Ⅲb型为导水管胶质瘤,其发生率较低,以梗阻性脑积水为首发症状,病理类型以低级别胶质瘤为主(图1J);Ⅲc型为NF1相关的BSG,可分布在脑干内任何部位,可表现出各种生长方式和影像学特点。

图1.基于MRI的脑干胶质瘤分型A.外生型;B.局灶内生型;C-E.弥散内生型脑干胶质瘤伴有局灶强化和高代谢;F-H.弥散内生型脑干胶质瘤无局灶强化和高代谢(C、H为11C-METPET-CT影像);I.顶盖胶质瘤;J.导水管胶质瘤。
二、根据DTI成像中皮质脊髓束(corticospinal tract,CST)和肿瘤的位置关系将BSG分为3型
A型:为推挤型,CST受到肿瘤推挤发生移位,患者四肢肌力为Ⅳ~Ⅴ级(图2)。
B型:为推挤+损害型,CST同时受到肿瘤的推挤和损害,患者受累肢体肌力为Ⅱ~Ⅲ级(图3)。
C型:为穿过型,CST从肿瘤内部穿过,患者受累肢体肌力为Ⅲ~Ⅴ级(图4)。
图2.DTI分型A型:肿瘤单纯推挤CST(推挤型)A.纤维束和肿瘤的三维重建结果,绿色为右侧的CST,肿瘤将CST推向左侧,患者的左侧肢体肌力为V-级;B-D.分别为磁共振T1WI轴位、矢状位以及冠状位与纤维束的融合图像,绿色为右侧的CST,红色为左侧的CST。

图3.DTI分型B型:肿瘤推挤并损害CST(推挤-损害型)A.纤维束和肿瘤的三维重建结果,粉红色为右侧的CST,可见CST明显受到肿瘤推挤发生移位,同时患者左侧肢体肌力为III级;B-D.分别为磁共振T1WI轴位、矢状位和冠状位与纤维束的融合图像,粉红色为右侧的CST。
图4.DTI分型C型:DTI穿过肿瘤(穿过型),红色和绿色分别表示左侧和右侧CST A,B.分别为磁共振T1WI轴位和冠状位,显示双侧CST均从肿瘤内部穿过;C,D.磁共振T1WI矢状位,分别显示在肿瘤内部穿行的左侧和右侧的CST(DTI为弥散张量成像,CST为皮质脊髓束)。
DTI成像所显示的纤维束是在数学模型基础上后期重建所获得的,纤维束形态和数量受图像采集和重建参数的影响较大。由于目前尚缺乏统一的技术标准,所以建议DTI作为制定手术入路的辅助性参考依据,术中应用可与电生理监测相结合。应用3.0 T MRI进行数据采集,采集图像时患者应保持头部静止,儿童患者无法配合时,建议在采集图像前30 min给予水合氯醛诱导睡眠。
病理学分类
一、组织病理学分类
目前,BSG的组织病理分类采用的是WHO(2007版)中枢神经系统肿瘤病理分类中胶质瘤的分类标准。BSG常见的组织病理类型包括:PAs、星形细胞瘤、少突星形细胞瘤、间变性星形细胞瘤、间变性少突星形细胞瘤和胶质母细胞瘤。肿瘤的病理类型和病理级别对指导后续治疗具有重要的参考价值(图5)。

脑干胶质瘤的咨询流程图。(注:手术前应常规行DTI检查,明确肿瘤和纤维束的位置关系)(NF1为I型神经纤维瘤病)
二、分子病理学分型
2016过渡版WHO中枢神经系统肿瘤病理分类中提出了“伴有H3 K27M突变的弥散型中线胶质瘤”,该类肿瘤主要见于儿童患者,病理以高级别胶质瘤为主。此外,本共识综合BSG的发病年龄和预后特点及目前分子遗传学方面的研究结果,建议将BSG分为4种分子亚型。
1.H3F3A K27M(编码组蛋白H3.3)突变型:H3F3A K27M为目前BSG中所发现的较高频突变,该类型BSG对放疗不敏感,易转移复发,预后较差。
2.HIST1H3B/C K27M(编码组蛋白H3.1)突变型:常见于年龄<5岁的DIPGs患者,相比于H3F3A K27M突变型预后较好,常伴有ACVR1突变。
3.IDH1突变型:仅见于成人,主要为非DIPGs,中位诊断年龄为43岁,预后较好。
4.其他类型:少部分患者并无IDH1/2、H3.3/3.1突变,为双阴型。对于该类患者的发病机制尚需进一步研究。
有条件的单位建议常规检测BRAF V600E、BRAF✌KIAA1549融合突变和IDH1/2、H3 K27M、PPM1D、TP53、ACVR1突变及MGMT启动子甲基化。以上分子病理结果可以判断预后。
参考资料来源:
脑千胶质瘤综合咨询中国专家共识编写委员会.脑干胶质瘤中国咨询共识家共识
- 文章标题:脑干胶质瘤影像学、病理学、分子学分型
- 更新时间:2020-07-28 16:36:24

 400-029-0925
400-029-0925