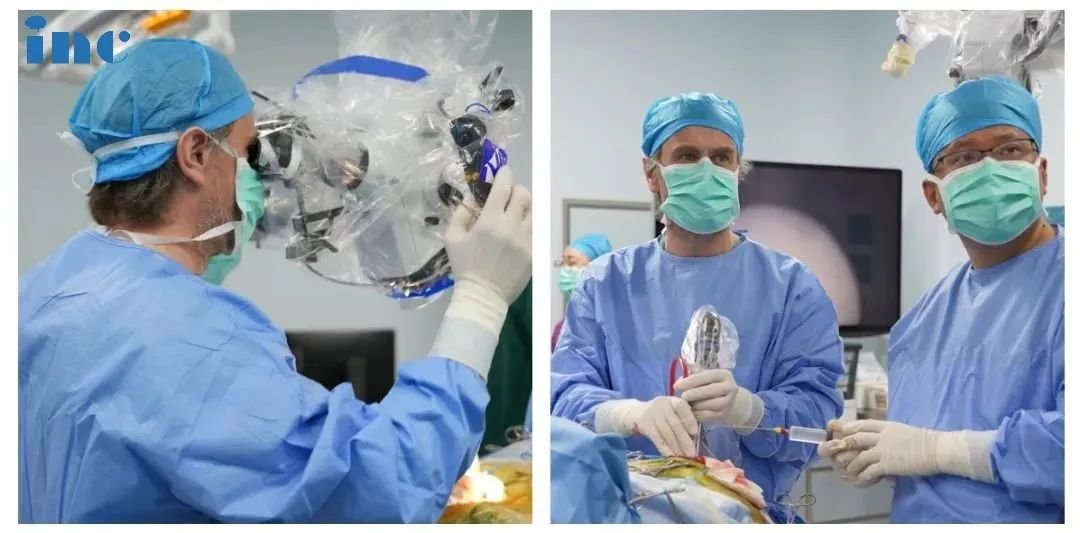
科学的进步与发展都离不提出新的作用,医学更如是......“双镜联合”手术教授INC福洛里希教授曾说过,“只了解一个手术入路远远不够”。

福洛里希教授接受INC专访时表示自己团队的优势之一是能够掌握颅底手术全部的入路
现代神经外科的进步史同时也是一部工具的进化史,神外显微镜的使用和发展,使得手术精确性大为提高,邻近组织的损害机会明显减少。而神经内镜的发展又进一步扩展了进入人脑的通道,将我们的视线扩大到显微镜下触难以触及的角落。神外显微镜+内镜“双镜联合”的手术方法更是将两种工具的优势放大,在确定手术顺利的前提下尽可能切除肿瘤。国际神经外科专家、国际神经外科联合会(WFNS)颅底手术委员会前主席、国际神外内镜高手、神经内镜“筷子技术”提出者INC法国Froelich教授更是国际神外领域内“双镜联合”使用的佼佼者。福教授多个经典手术案例,深度解读这些前沿技术……

52岁女士较大蝶窦-海绵窦脑膜瘤,如何才能顺利手术?
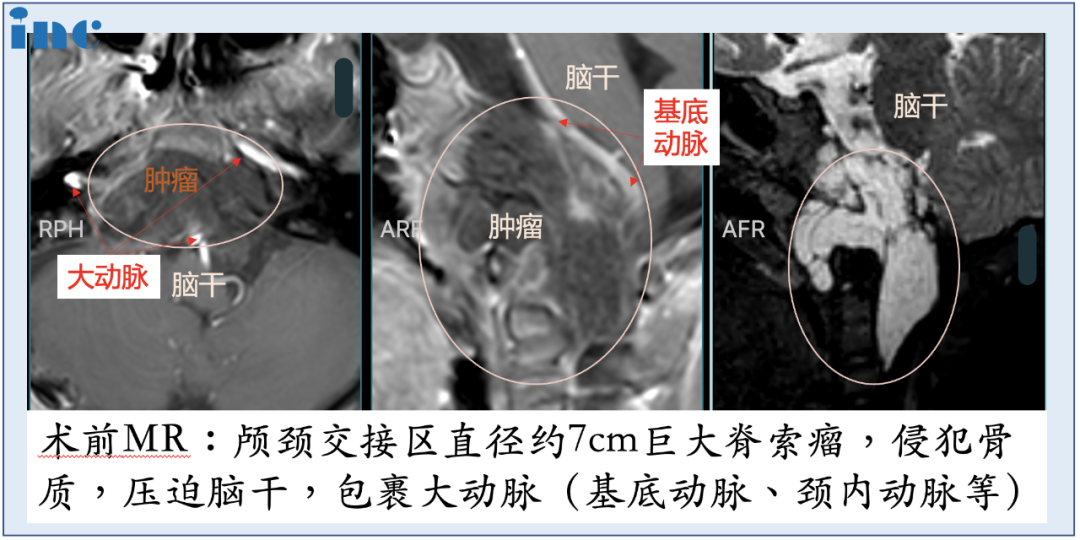
52岁女性Aude出现三叉神经痛和面部感觉麻木。MRI显示海绵窦区脑膜瘤,向颞窝延伸浸润,进入蝶腭窝和蝶窦。6个月内肿瘤明显生长,手术切除肿瘤是当务之急!
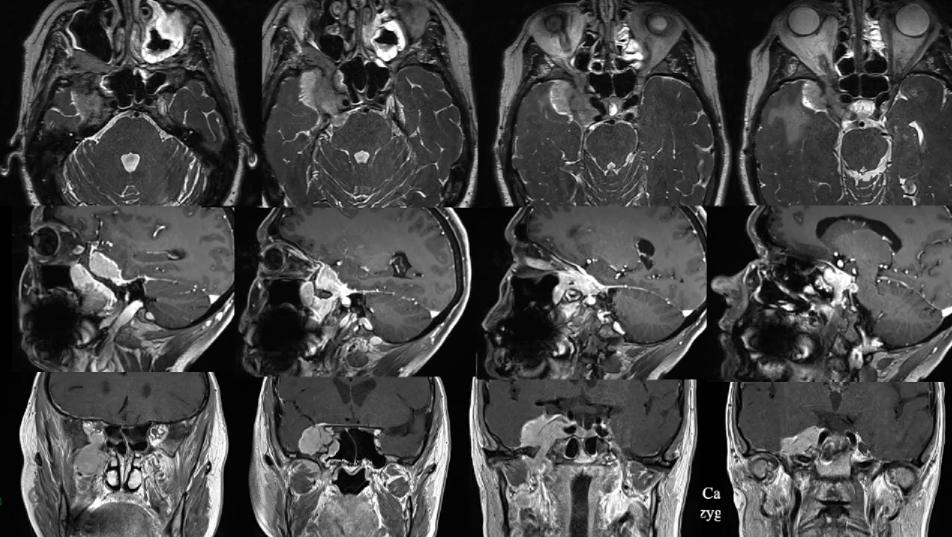
手术前影像
然而,一道难题摆在了身经百战的神外医生面前。Aude这样大小的垂体肿瘤已属较大,按照传统的手术方案,这样手术一般会分开2次手术,但对于大多数患者来说,较好一次手术切除肿瘤!鉴于这样复杂的颅内外沟通性生长的复杂脑膜瘤,福洛里希教授详细咨询及手术评估后,制定了如下治疗策略:

福洛里希教授治疗策略
1.首前沿行手术切除海绵窦外肿瘤,将颅外蝶窦、蝶腭窝肿瘤全切,减小肿瘤负荷,进行肿瘤控制
2.海绵窦内肿瘤和神经、血管生长密切,如要进行手术切除,对颅神经损伤明显,可造成面瘫、眼睑闭合不全等并发症风险大,故建议海绵窦内肿瘤进行放疗控制。
3.为了为Aude制定较为周全的手术方案,福教授经过缜密的考量,决定为她开展神外内镜+显微镜“双镜联合”手术治疗。
,Aude的手术顺利完成,无任何神经损伤、加上后期的辅助治疗,术后随访16个月没有肿瘤进展复发迹象。
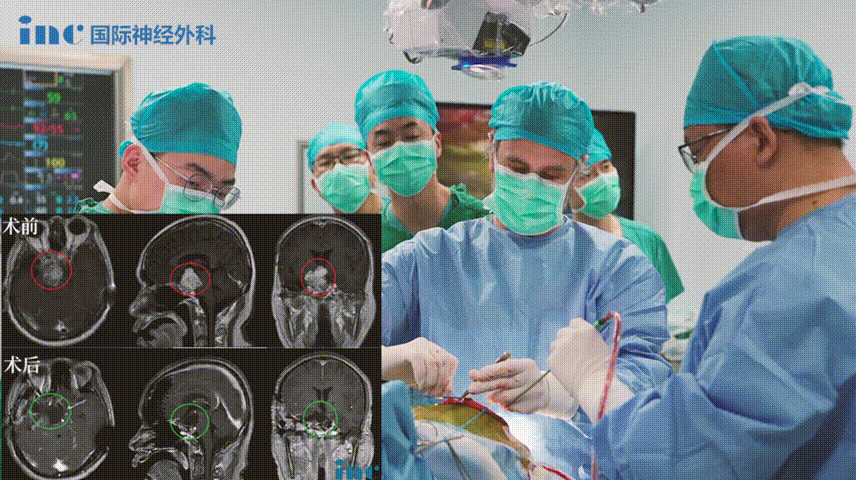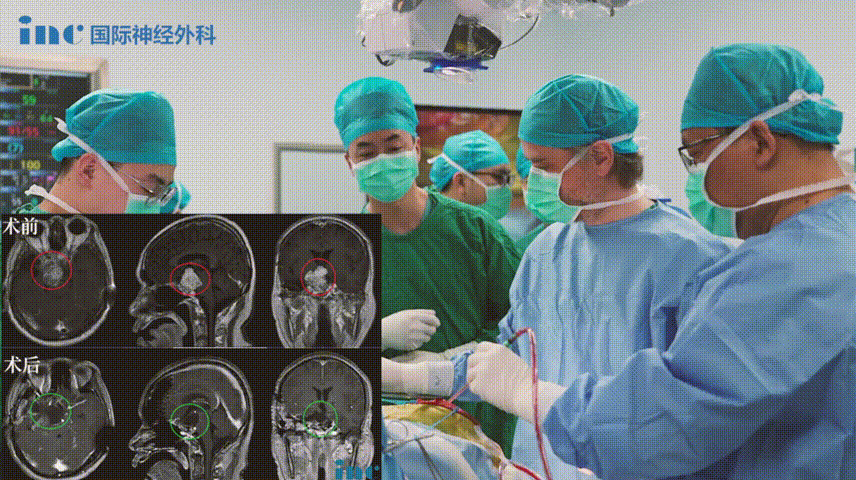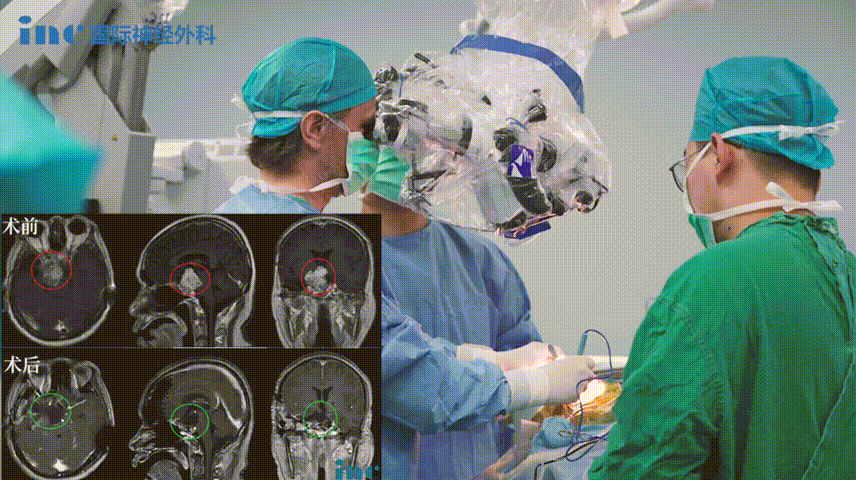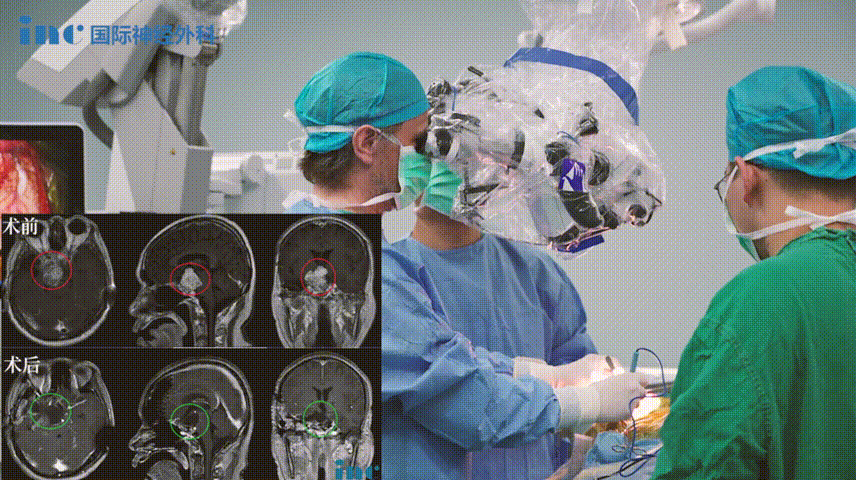
福洛里希教授手术术中纪实
▼使用颧弓入路手术,利用筷子技术神经内镜+显微镜次全切除肿瘤,从海绵窦剥离硬脑膜,切除了浸润的硬脑膜和向颞部延伸的硬膜上脑膜瘤。
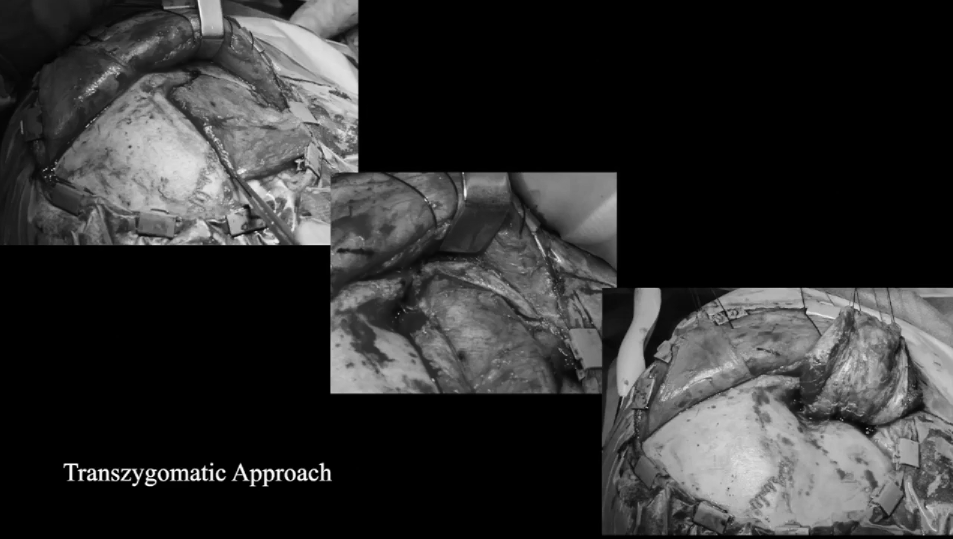
▼显微镜下暴露海绵窦外侧壁,注意暴露血管,并进行窦外肿瘤切除。

▼显微镜下切除部分肿瘤或瘤内减压

▼显微镜下暴露充分肿瘤,进行关键解剖定位
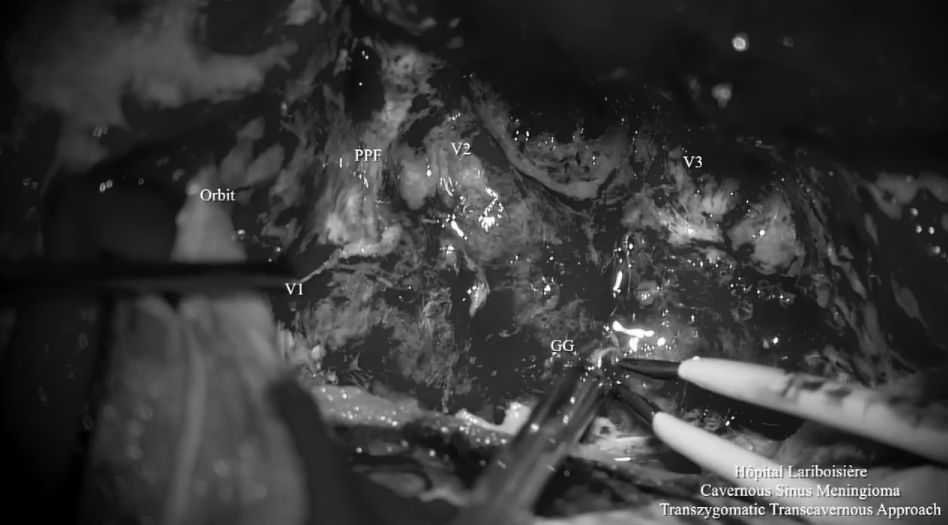
▼利用OPC间隙(orbitopterygopalatine corridor)进入蝶窦,发现肿瘤突出到窦内,暴露V2神经的侧面。神经内镜下对蝶窦中的肿瘤进行切除,这种方法可以切除硬膜内间隙和鼻窦中的肿瘤。为保留关键神经功能,海绵窦内的肿瘤没有切除。


▼切开眶肌
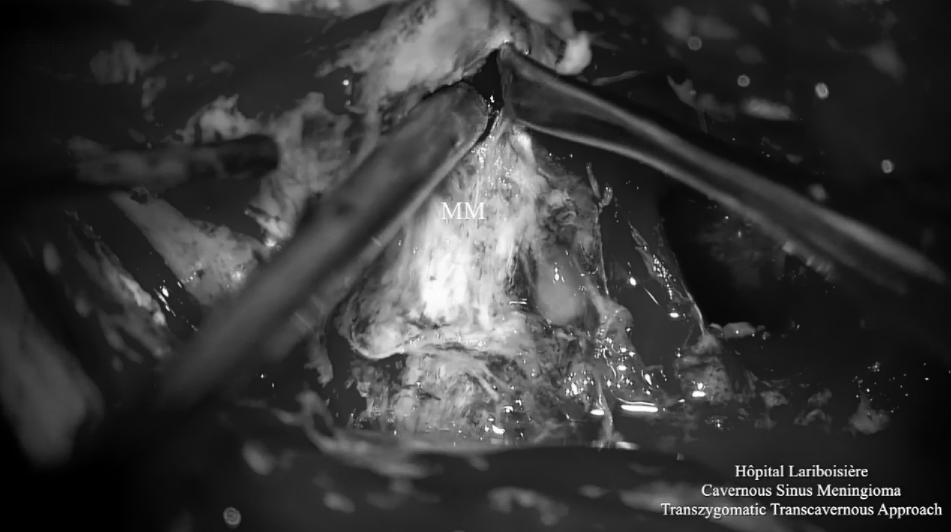
▼神经内镜操作下暴露和切除肿瘤
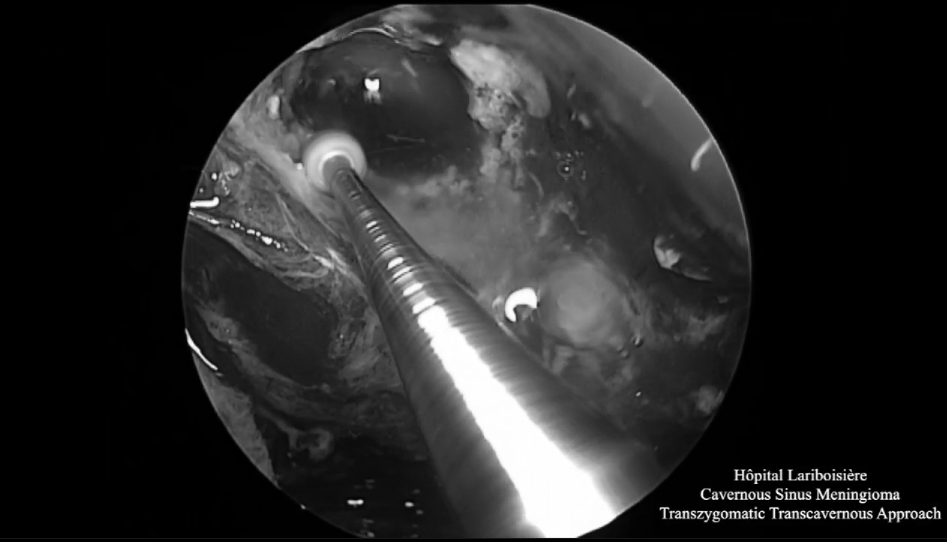
▼神经内镜下切除肿瘤后的术野
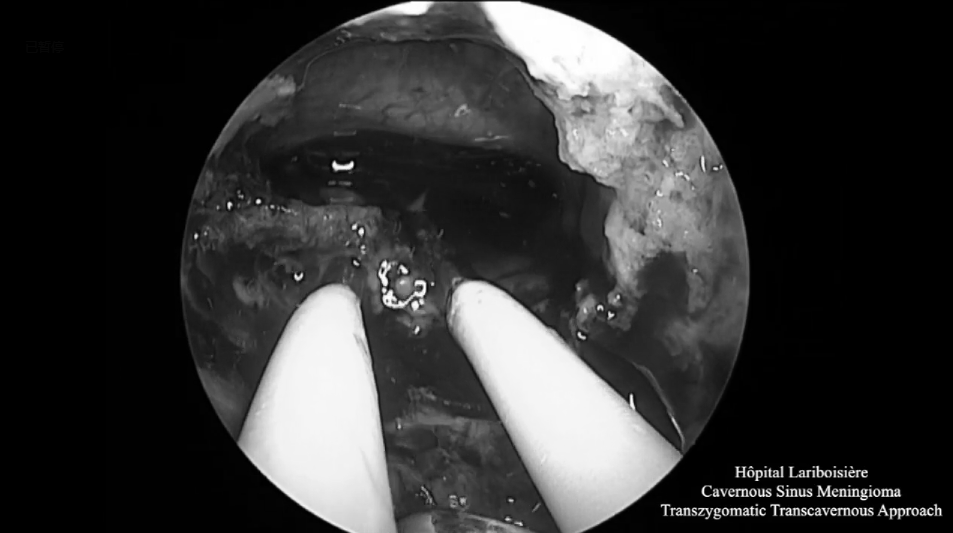
▼术腔使用自体脂肪填充

完成肿瘤切除后,闭合蝶窦。术后恢复好,无新发神经功能障碍,V2-视神经功能没有恶化。术后组织病理学为I级脑膜瘤,Ki-67指数为10%。结合患者术前肿瘤生长迅速,患者在术后3个月接受了放射外科手术。患者在放射外科手术后16个月没有进展迹象。
该国际治疗案例3大解读
1、KI67指数和脑膜瘤治疗策略、预后关系解读
人们普遍认为Ki-67 PI与复发相关,但该认识并非基于长期随访的基于人群的连续数据。实际上,先前的文献报导是存在有相互矛盾的,目前也有小部分学者对此是质疑态度的。今年一篇发表于神经外科顶刊Neurosurgery的文章研究报导了,Ki-67是复发的合适评估因子,长期随访表明,Ki-67是何时可能复发而不是脑膜瘤是否复发的标志。长期随访策略需要考虑切除范围和肿瘤增长率,而Ki-67能够很好地反映增长率,研究结果不支持将高Ki-67指数定义为复发风险组。

Ki67指数和脑膜瘤放疗与否?脑膜瘤的治疗一般以手术切除为主,根据的脑膜瘤治疗指南,WHO1/2级脑膜瘤全切术后不予放疗,术后有残留予以放疗辅助。WHO3级不论手术切除程度建议予以放疗。同时若有Ki67指数高,部分医师也会结合患者情况建议术后放疗。外科手术切除是脑膜瘤的优选治疗方式,其治疗效果是伽玛刀所无法具备的。但对于因为以下情况而无法手术的患者而言,可以采用伽玛刀进行治疗。
2、海绵窦脑膜瘤手术难度解读
海绵窦(CS)的平均尺寸为2厘米长,1厘米宽;该区域神经、血管交错解剖高度复杂,涉及多支颅神经、重要脑动脉、较大静脉丛和脑干;因此海绵窦脑膜瘤被称为较难以治疗的脑膜瘤之一,1980年以前,该区域几乎被视为“手术禁区”,手术伴有较高的死亡率和致残率。尽管在七十年代显微外科技术得到了发展,但人们认为显微神经外科在处理海绵窦内及周围的病变方面已经达到了较限。损伤神经结构的较,以及引起无法控制的出血或术后脑脊液漏似乎是一个不可避免的难题。
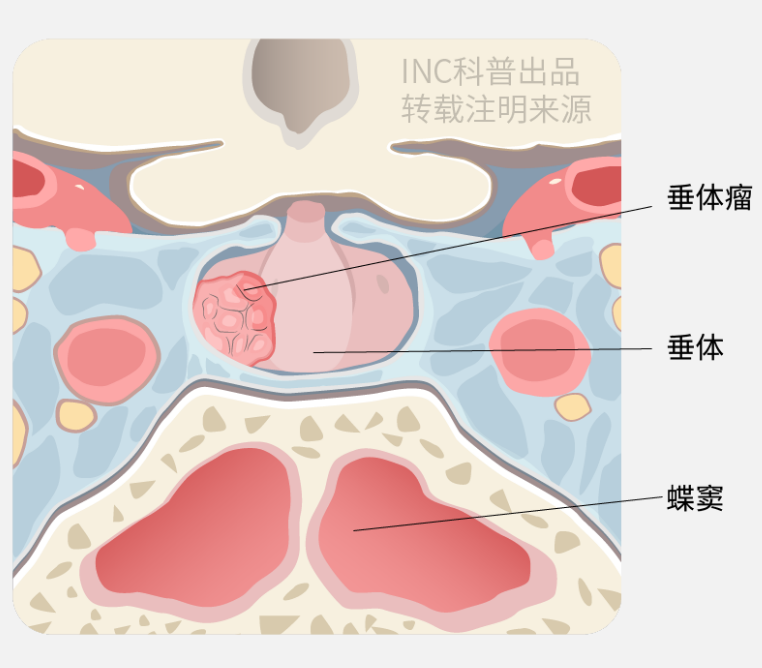
图示蓝色区域为海绵窦,海绵窦包围垂体复合体,包含颅神经(CNs)III、IV、V1、V2和VI,颈内动脉(ICA)的海绵段和颈动脉周围交感神经丛。颅神经III、IV和VI被蛛网膜鞘和蛛网膜颗粒包围,海绵窦内脑膜瘤由此产生。
海绵窦及其周围病变是神经外科“技术难度较大的”,该区域神经、血管交错解剖高度复杂,涉及多支颅神经、重要脑动脉、较大静脉丛和脑干。1980年以前,该区域几乎被视为“手术禁区”,手术伴有较高的死亡率和致残率。20世纪80年代初,国际Dolenc入路和Dolenc三角创始人Vinko V.Dolenc教授和Hakuba教授使Parkinson的直接手术方法重新焕发了活力,介绍了从硬膜内和硬膜外直接进入海绵窦的显微手术技术。
3、国际前沿技术解读-筷子神经内镜+显微镜双镜联合技术要点
“双镜联合手术的技术使用,可以在同一台手术中发挥取长补短的优势,充分利用内镜的纵深、角度优势与显微镜下的立体视野和操作空间优势,根据病变的位置、大小和性质,同时进行肿瘤的切除和双向修补,规避了单一手术可能会带来的等技术的不足之处。打个比方,显微镜就像海水表面的战斗机,内镜就像是海里的潜艇,双者联合作战就有了三维打击航空母舰的战斗力。”
双镜联合颅底手术是联合运用显微镜和神经内镜技术。其中,显微镜下的显微神经外科技术目前是成熟的颅内肿瘤手术技术,适合于传统开颅手术的实施。神经内镜技术是近几十年来逐步取代传统方式,成为中线颅底部位手术的常规治疗方式,是对于侵袭性垂体瘤,改变了以往经蝶手术在中手术视野不足,操作不便的困难。但两种技术都存在一点的局限性,其中经颅显微镜下的手术由于视角、手术方向等因素,使其处理突向三脑室方向和鞍内方向的病变时,通常较为困难。而内镜技术在处理鞍内病变时具有明显优势,其次当病变往三脑室方向生长,经鼻入路是较佳的手术通道,无重要神经血管结构的阻挡。假若病变向侧方生长,内镜的操作将受到很大的限制,而显微镜由于是侧方视野,可以合适地处理此类病变,并且在立体视野的分离操作也是显微镜技术的优势。双镜联合手术的技术要点在于充分利用两种不同技术的技术特点,起到扬长避短的效果。

 400-029-0925
400-029-0925