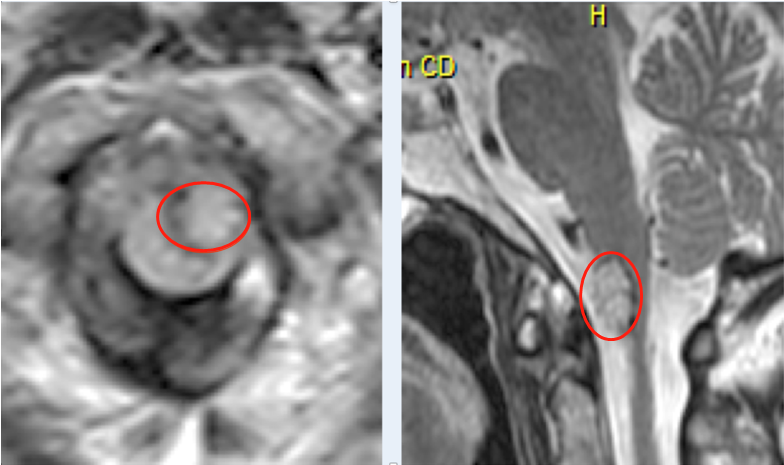
胶质瘤不同类型基因治疗的临床试验证实基因治疗是顺利的。脑肿瘤一般局限于脑部,很少转移到其他组织;故可以直接针对胶质瘤中分裂的肿瘤细胞(大多数脑细胞是有丝分裂后期的)进行治疗,以此来控制肿瘤的生长。胶质瘤的独特性使其成为基因治疗的目标。

1条件细胞毒性基因
有条件细胞毒性基因治疗的目标是将较初的非细胞毒性酶递送到肿瘤细胞中,然后没有毒性的前药通过相应的酶转化为细胞毒性代谢物。由于并非全部肿瘤细胞都能表达靶酶,因此其功效很大水平上取决于所谓的“旁观者效应”;其中毒性代谢物能够扩散并作用于周围的肿瘤细胞。该疗法可控制血管生成并产生抗肿瘤作用。
1.1单纯疱疹病毒-胸苷激酶(herpes simplex virus-thymidine kinase,HSV-TK)/更昔洛韦(ganciclovir,GCV)系统
HSV-TK/GCV系统已在临床前和临床上进行了广泛的基因治疗研究。在该系统中,GCV不能被哺乳动物的TK磷酸化,但是病毒的TK可以使其磷酸化。HSV-TK可将GCV转化为GCV的毒性磷酸化代谢产物,从而控制S期细胞的DNA合成并引发细胞凋亡。虽然GCV三磷酸不能穿过细胞膜,但可以通过间隙连接分布并引起旁观者效应。
在接受HSV-TK/GCV基因治疗的胶质母细胞瘤患者中也显示出抗肿瘤免疫反应;与对照组相比,接受基因治疗的患者的白细胞介素(interleukin,IL)-12和干扰素-γ(interferonγ,INF-γ)水平升高,这与肿瘤细胞坏死后血液中释放的抗肿瘤抗原的免疫系统激活有关。
1.2CD/5-FC系统
胞嘧啶脱氨酶/5-氟胞嘧啶(cytosine deaminase/5-fluorocytosine,CD/5-FC)是另一种有前景的酶/前药组合。当5-FC用作CD底物时,所得的5-氟尿嘧啶(5-fluorouracil,5-FU)产物控制胸苷酸合成酶,导致细胞死亡。由于5-FU可自由扩散到周围的肿瘤细胞中,基于CD的基因治疗能够引起肿瘤消退伴随强大的旁观者效应;并且已经在大鼠神经胶质瘤模型实验中显示出其效果。
1.3其他系统
另一个系统是兔羧酸酯酶(rabbit carboxylesterase,rCE)/伊立替康系统。与人羧酸酯酶相比,rCE能更合适地将伊立替康转化为细胞毒性药物7-乙基-10-羟基喜树碱;后者是一种毒性更强的物质,能强烈控制拓扑异构酶Ⅰ。此外,还有脱氧胞苷激酶(deoxycytidine kinase,dCK)/阿糖胞苷(cytarabine Arabinoside,AraC)系统,dCK可将AraC转化为Ara-胞苷-5'-三磷酸,控制DNA合成。
2靶向毒素
在一些胶质瘤亚型中,肿瘤细胞上的特异性受体的过表达为胶质瘤的靶向治疗提供了较好的途径。这些特异性受体主要包括表皮生长因子受体Ⅲ型突变体(epidermal growth factor receptor variantsⅢ,EGFRvⅢ)抗体、IL-13Rα2、尿激酶型纤溶酶原激活物(urokinase type plasminogen activator,uPA)、转铁蛋白和其他几种多肽。
在靶向毒素方法中,靶受体的天然配体与细胞毒性细菌产物如假单胞菌(pseudomonas,PE)和白喉外毒素(diphtherotoxin,DT)的催化和易位结构域融合。由于这些特异性受体在正常脑组织中几乎不存在,因此这是一种具吸引力的治疗策略,而且其潜在的副作用很小。通过这种方式,在过表达靶向受体的肿瘤细胞中选择性地控制蛋白质合成,而使正常的神经细胞免于细胞毒性作用。
3靶向胶质瘤的转基因
胶质瘤基因治疗的另一种策略是特异性靶向肿瘤发生,以阻止肿瘤的生长。新毛细血管的形成,是恶性肿瘤的标志性特征。其可以通过递送抗血管生成基因或通过降低促血管生成因子的表达来靶向治疗。大量抗血管生成基因已被用于胶质瘤基因治疗,包括编码脑特异性血管生成控制剂(brain specific angiogenesis inhibitors,BAI)、血管抑素、内皮抑素、血栓反应素、组织金属蛋白酶控制剂(tissue inhibitor of metalloproteinase,TIMP)、C-X-C基序趋化因子配体4(C-X-C motif chemokine ligand 4,CXCL4)和IL-12。
编码血管内皮生长因子(vascular endothelial growth factor,VEGF)、成纤维细胞生长因子(fibroblastgrowthfactor,FGF)和IL-8的促血管生成基因都是基因治疗的潜在靶点。另外,通过编码DNA修复蛋白MGMT的失活以提高烷化剂替莫唑胺(temozolomide,TMZ)的治疗效果,也能达到治疗胶质瘤的作用。递送TP53肿瘤抑癌基因也被认为是一种可行的基因治疗方法。
4免疫调节治疗基因
免疫系统是一种强有力的内源性资源,可以抗肿瘤生长。活性多克隆抗肿瘤免疫应答具有长期免疫记忆的潜力,并具有清除手术后残留的耐药和抗原丢失的肿瘤细胞的能力。众所周知,胶质瘤在抗肿瘤免疫治疗上存在许多特有的障碍,其中包括由于中枢神经系统的血-脑屏障(blood brain barrier,BBB)和缺乏经典抗原呈递细胞(antigen presenting cell,APC)限制了胶质瘤的免疫治疗;同时,胶质瘤微环境中的免疫控制细胞因子和细胞亚群也抵消合适的抗肿瘤免疫反应。然而,这些并非的障碍,在高级别胶质瘤(high grade gliomas,HGG)中增加BBB的通透性有利于淋巴细胞浸润。
广泛的临床前研究证据表明,肿瘤的免疫控制性微环境可被逆转以产生合适的抗肿瘤免疫应答。IL-2、IL-12、IL-4、IFN-γ、IHF-α、β和肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)都是细胞因子途径的免疫调节基因治疗的候选者。另一方面,利用表达Fms样酪氨酸激酶3(Flt3)配体的ADV载体募集免疫细胞策略可将树突状细胞(dendritic cell,DC)和其他APC募集到脑肿瘤中。将此方法与提高胶质瘤抗原免疫原性的方法相结合,是产生合适抗肿瘤免疫应答的潜在策略。
- 文章标题:胶质瘤的治疗基因
- 更新时间:2021-11-11 13:53:07

 400-029-0925
400-029-0925