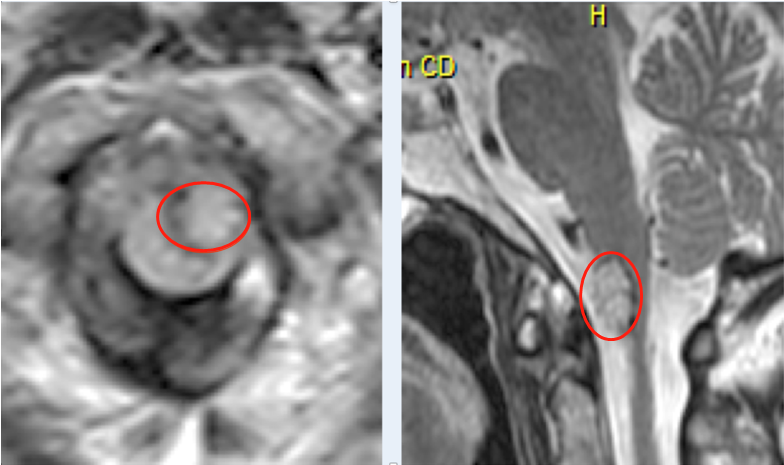
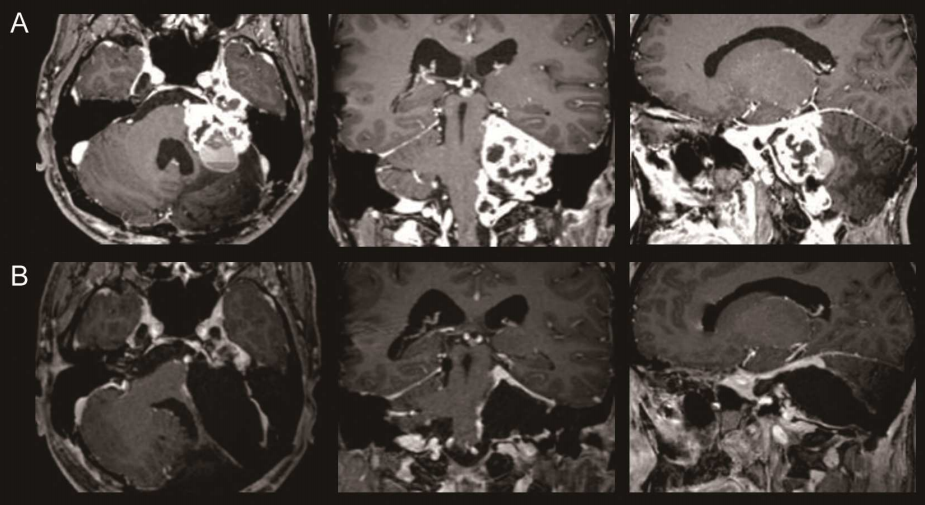
髓源性控制细胞在脑胶质瘤中的表达及特点,近年来,免疫治疗在实体瘤中的研究及应用备受关注,其中肿瘤诱导的免疫控制在免疫治疗中起重要作用。髓源性控制细胞作为控制性免疫细胞的一个类别,其同样影响着脑胶质瘤的发生、发展。目前研究表明:髓源性控制细胞在多种肿瘤病人的外周血和肿瘤组织中的表达增加,其通过高表达精氨酸酶-1(arginase1,ARG-1)、诱导型一氧化氮合酶、活性氧类等,诱导免疫控制因子(如IL-10)分泌及调节性T细胞(T regulatory cells,Treg)产生,进而控制机体抗肿瘤作用,促进肿瘤进展。中枢神经系统中血-脑屏障可在程度上限制外周血中髓源性控制细胞向脑胶质瘤浸润,但髓源性控制细胞在脑胶质瘤中仍发挥着重要的免疫控制功能。
1髓源性控制细胞在脑胶质瘤病人外周血和肿瘤组织中的表达差异
GIELEN等的研究表明:胶质母细胞瘤(glioblastoma,GBM)病人血液中的M-髓源性控制细胞和PMN-髓源性控制细胞较健康对照组明显增加,且胶质瘤细胞悬液中的髓源性控制细胞完全由CD15+PMN-髓源性控制细胞组成;MOYES等的研究发现:脑胶质瘤组织中CD15+细胞主要分布在血管周围;这也在程度上反应髓源性控制细胞可透过血-脑屏障由血液向肿瘤组织浸润。另有研究表明:在GBM中82%为CD14-CD15+PMN-髓源性控制细胞,其次是lin-e-髓源性控制细胞(15%)和M-髓源性控制细胞(3%)。
在GBM病人外周血中,髓源性控制细胞仍以PMN-髓源性控制细胞为主,且具有较高的T细胞控制能力。脑胶质瘤病人外周血及肿瘤组织内髓源性控制细胞的含量及亚型存在差异性:一方面,可能由于髓源性控制细胞不同亚型的构象差异性导致血-脑屏障通过率不同;另一方面,髓源性控制细胞不同亚型可能不同程度受到肿瘤细胞分泌的细胞因子、趋化因子的调控。
2髓源性控制细胞在脑胶质瘤中的浸润、聚集
在肿瘤微环境中存在着多种细胞因子、趋化因子,其除作用于肿瘤细胞外,还可直接或间接影响肿瘤微环境中免疫细胞的浸润和聚集。CC趋化因子-2(C-C chemokine ligand 2,CCL-2)作为一种趋化因子,可由肿瘤来源的CCL-20和骨保护素诱导小胶质细胞和巨噬细胞分泌产生,并分别通过CCR4和CCR2招募M-髓源性控制细胞参与胶质瘤微环境的免疫控制。
有研究表明:CCL-2的表达水平与病人总生存期及胶质瘤恶性程度呈相关性,这也进一步证明CCL-2在髓源性控制细胞的瘤内浸润过程中起重要调控作用。此外,半乳糖凝集素1(galectin1,Gal-1)作为胶质瘤细胞分泌的细胞因子之一参与先天性及适应性抗肿瘤免疫过程。BAKER等证实与表达Gal-1的GL261胶质瘤相比,未表达Gal-1的肿瘤组织内髓源性控制细胞的浸润水平增加约7倍,其可诱导大量自然杀伤细胞向肿瘤组织内浸润并发挥抗肿瘤作用;且髓源性控制细胞浸润主要发生在早期Gal-1缺陷的胶质瘤。
除肿瘤微环境中的细胞因子、趋化因子对髓源性控制细胞浸润起调节作用外,LIAO等认为外源性因素(如地塞米松)同样可以促进髓源性控制细胞向胶质瘤组织内浸润,并可上调髓源性控制细胞的控制活性;但也有学者认为地塞米松与髓源性控制细胞的瘤内浸润没有相关性,也没有发现地塞米松治疗时间影响钙结合蛋白S100A8/9或精氨酸酶表达。这种差异可能是由于地塞米松对髓源性控制细胞浸润的调节作用与肿瘤恶性程度有关。
有研究发现:在WHOⅠ级胶质瘤和GBM组织中,地塞米松对髓源性控制细胞向瘤内浸润的促进作用要优于非肿瘤性脑组织和WHOⅡ~Ⅲ级胶质瘤。这些结果表明:地塞米松可在程度上促进髓源性控制细胞在血液中的聚集及其向肿瘤组织浸润,并且与肿瘤恶性程度具有潜在相关性。但地塞米松在髓源性控制细胞的分化、迁移及浸润中的具体机制尚需进一步深入研究。
3髓源性控制细胞在脑胶质瘤中的免疫控制功能
肿瘤免疫逃逸的机制之一即为肿瘤微环境中髓源性控制细胞的扩增,深入了解髓源性控制细胞所发挥的免疫控制功能,可以为进一步开展免疫治疗提供前提和基础。DUBINSKI等发现肿瘤来源的CD4+效应记忆T细胞可高水平表达程序性细胞死亡蛋白1(programmed cell death protein 1,PD-1),其配体PD-L1在胶质瘤相关PMN-髓源性控制细胞上的表达也明显上调;这提示PMN-髓源性控制细胞可能通过参与PD-1/PD-L1免疫检查点控制机制阻碍T细胞增殖,而发挥其在GBM中的免疫控制功能。
胶质瘤干细胞样细胞高水平产生巨噬细胞迁移控制因子(macrophage migration inhibitory factor,MIF),并可通过受体CXCR2依赖的方式增加髓源性控制细胞中ARG-1的表达,降低瘤内细胞毒性T细胞(cytotoxic T lymphocyte,CTL)浸润,进而下调CTL对肿瘤细胞的杀伤效应。同时,有研究证实:血液来源的PMN-髓源性控制细胞是目前表达ARG的主要细胞群,且对T细胞功能产生很强的控制作用。此外,CD124可介导IL-13诱导髓源性控制细胞产生ARG,并以IL-4Ra依赖的方式控制T细胞增殖,从而实现髓源性控制细胞介导的免疫控制。因此,血浆中ARG-1和粒细胞集落刺激因子(granulocyte colony stimulating factor,G-CSF)水平升高可能在促进髓源性控制细胞控制因子的功能发挥及扩增方面起到重要调控作用,进而产生免疫控制效应。
有研究表明:用环氧化酶-2(cyclo oxygenase-2,COX-2)控制剂可控制腺素2(PGE2)的产生,进而降低肿瘤微环境中髓源性控制细胞的扩增,且髓源性控制细胞扩增降低的效应与肿瘤微环境中CXCL-10和CTL增加具有一致性。因此,髓源性控制细胞可通过参与COX-2-PGE2途径而限制瘤内CTL浸润,进而在胶质瘤细胞的发育过程中发挥免疫控制作用。
综上:髓源性控制细胞作为肿瘤微环境中免疫控制细胞的一个亚群,其通过参与多种途径发挥控制T细胞活性的功能,进而促进肿瘤细胞的免疫逃逸过程。因此,通过干预或解除髓源性控制细胞的功能发挥,势必可以在程度上为免疫治疗奠定疗效基础。
4靶向髓源性控制细胞脑胶质瘤的免疫治疗
在胶质瘤免疫微环境中,髓源性控制细胞在多种因素作用下聚集和活化,控制机体抗肿瘤免疫作用,参与肿瘤免疫逃逸;因此,以直接或间接形式靶向髓源性控制细胞的免疫治疗或许可为脑胶质瘤的免疫治疗提供新思路。由于胶质瘤干细胞样细胞产生的MIF可通过受体CXCR2依赖的方式增加髓源性控制细胞中ARG-1的表达,并降低瘤内浸润的CTL,当使用MIF控制剂萝卜硫素时,可控制正常CD14+单核细胞向髓源性控制细胞的转化;因此,靶向肿瘤来源的MIF可在降低瘤内浸润髓源性控制细胞的同时增加瘤内CTL浸润,进而发挥抗肿瘤作用。
此外,有研究表明:通过降低肿瘤组织中Gal-1表达可减少瘤内浸润的髓源性控制细胞,并延长荷瘤鼠的生存期;COX-2通路促进髓源性控制细胞扩增及其在肿瘤微环境中的积累,限制CTL的瘤内浸润并促进胶质细胞发育;趋化因子CCL-2可分别通过CCR4和CCR2募集M-髓源性控制细胞向瘤内浸润,这在动物实验中已得到证实。
目前已证实:对T细胞淋巴瘤合适的人源性CCR4脱胶抗体Mogamulizumab已在实体瘤Treg靶向治疗的iA期临床试验中得到应用。因此,靶向肿瘤微环境中细胞因子、趋化因子途径可减少髓源性控制细胞向瘤内的浸润、积累,进而解除瘤内浸润T细胞的活性控制,从而可以控制肿瘤发生、发展,为机体的抗肿瘤免疫奠定基础。
- 文章标题:髓源性控制细胞在脑胶质瘤中的表达及特点
- 更新时间:2021-11-11 10:40:28

 400-029-0925
400-029-0925