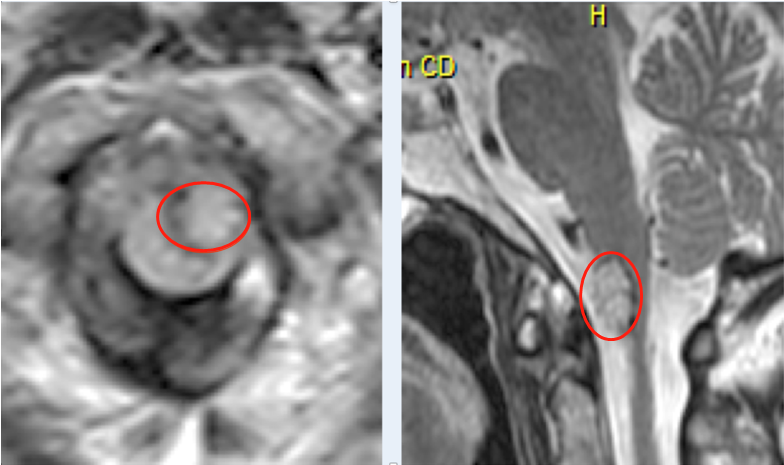
1分级诊断
胶质瘤的分级诊断以及对瘤体不同成分(如出血、水肿等)的评估对于提供治疗决策和评估预后至关重要。目前人工智能领域已经有大量的工作涉及胶质瘤高低级别的分级诊断。基于人工智能的计算机辅助诊断系统(computer-aided diagnosis system,CAD)可以辅助放射科医生的诊断工作。
Hsieh等研发的CAD应用GLCM提取纹理特征,用以评估高低级别胶质瘤(AUC0.89,准确度87%),应用该系统后放射科医师诊断准确度有明显提高(AUC从0.81提高至0.90),证明该CAD不仅能够辅助区分高低级别胶质瘤,还能够提高放射科医师诊断的准确度,为人工智能走向临床奠定基础。
2鉴别诊断
不典型胶质瘤有时与其他肿瘤难以鉴别,例如颅内淋巴瘤、转移瘤等。Artzi等回顾性分析439例胶质母细胞瘤和脑转移瘤病人的MRI特征,基于SVM等分类器建立评估模型,SVM模型评估组平均敏感度为0.86,AUC为0.96,并可以进一步鉴别胶质母细胞瘤和脑转移瘤亚型。Zacharaki等对MR影像进行特征提取、特征选择后,实现不同类型如胶质瘤、转移瘤及脑膜瘤等鉴别诊断,其准确度、敏感度和特异度分别为85%、87%和79%。Kunimatsu等开发基于纹理特征的算法,通过对脑胶质瘤及原发中枢神经系统淋巴瘤T1WI增强影像进行纹理分析,实现辅助胶质瘤与原发中枢神经系统淋巴瘤的鉴别作用,该算法在训练集内的AUC较高可达0.99。
3预后分析
肿瘤异质性发生在分子水平,但异质性可以通过医学影像中观察到的纹理宏观反映,不同异质性的肿瘤预后可有明显差别。为了研究胶质母细胞瘤病人肿瘤异质性与病人生存时间的关系,Liu等分别从长期生存和短期生存胶质瘤病人的T1WI增强影像中提取了3种类型的纹理,随后使用SVM学习不同纹理类型与肿瘤异质性的关系,评估结果证明可以通过纹理特征评估肿瘤的异质性程度,从而评估病人生存周期,但研究表明仍需要对算法进行进一步优化来提高对于生存周期分组的准确性。
Emblem等进一步将确诊胶质瘤病人的生存期分为4组(6个月,1、2、3年),基于肿瘤MR影像直方图特征训练SVM,测试组的SVM测试结果AUC为0.794~0.851,结果证明SVM可以实现根据影像精确评估生存期。
4疗效监测
恶性胶质瘤术后须放化疗治疗,但目前存在的一个问题是无法评估病人放化疗后的疗效反应。Kickingereder等从复发胶质母细胞瘤病人的影像中提取了4842个特征用以生成评估模型,用以对实验组病人的无病进展生存期和总生存期进行分层。另一个较大的问题是难以区别治疗后肿瘤进展(true tumor progression,TTP)和假性进展(pseudo progression,PSP)。Qian等根据这一临床现状,应用稀疏字典学习模型区分TTP及PSP的影像特征并用实验组加以验证,平均准确度为0.867,AUC0.92。由此可见,该模型有望辅助临床TTP及PSP的早期诊断,辅助监测胶质母细胞瘤的治疗效果。
另外,传统MRI定性方法难以确定高级别胶质瘤的浸润边缘,而Chang等开发了一个全自动系统,纳入36例具有病理结果的MR影像训练CNN模型,发现CNN可生成细胞密度图谱,从而实现无创性识别胶质瘤浸润边缘,这有利于病人的病情评估、胶质瘤治疗的疗效监测以及外科手术的进行。
5分子水平诊断
影像基因组学表明影像特征与肿瘤基因、蛋白质和分子改变息息相关,但其中隐含的信息仅依靠人眼并不能够完全捕获。人工智能算法可以辅助高效、准确地挖掘影像的潜在信息,从而将宏观影像特点与微观基因表达类型相关联,可更加精确地指导临床,实现胶质瘤的个体化治疗,且较人工诊断具有明显优势。胶质瘤常见的基因突变有异柠檬酸脱氢酶(isocitrate dehydrogenase,IDH)、表皮生长因子受体(epidermal growth factor receptor,EGFR)等,不同的分子亚型在肿瘤的好发位置、治疗敏感性等方面各有不同。IDH1突变被认为与胶质瘤的生存期关系密切。
Wu等应用基于影像组学的分类模型评估IDH1突变状态的胶质瘤,结果显示RF具有较高的评估性能(平均准确度0.885,AUC0.931)。α地中海贫血伴智力低下综合征(X-linked alpha thalassemia mental retardation syndrome,ATRX)基因表达对于低级别胶质瘤分子分层具有临床意义。Ren等基于液体衰减反转恢复(FL人工智能R)序列提取影像特征建立SVM评估模型,评估ATRX(-)的病人的准确度、AUC、敏感度、特异度分别为91.67%、0.926、94.74%、88.24%,亦证明该SVM评估模型可实现无创性评估低级别胶质瘤ATRX基因表达。O6-甲基鸟嘌呤-DNA甲基转移酶(O6-methyl guanine-DNA methyl transferase,MGMT)的甲基化与胶质瘤的瘤周水肿相关。
MGMT有助于DNA修复,甲基化MGMT则会控制DNA修复,从而导致胶质母细胞瘤对化疗药耐受。Korfiatis等根据这一理论依据提取相关影像学纹理特征,结合SVM及RF分类器实现了评估胶质母细胞瘤MGMT甲基化状态,亦证明影像学有可能成为简便易行的无创性胶质母细胞瘤MGMT甲基化的生物标志物。染色体1p/19q联合缺失的胶质瘤的影像表现具有的特点,且1p/19q联合缺失的低级别胶质瘤病人治疗反应好,生存期更长。Akkus等应用CNN评估MR影像中胶质瘤的1p/19q染色体表型状态,评估结果敏感度93.3%、特异度822%、准确度87.7%。
- 文章标题:人工智能在胶质瘤诊断中的应用
- 更新时间:2021-11-09 15:01:02

 400-029-0925
400-029-0925