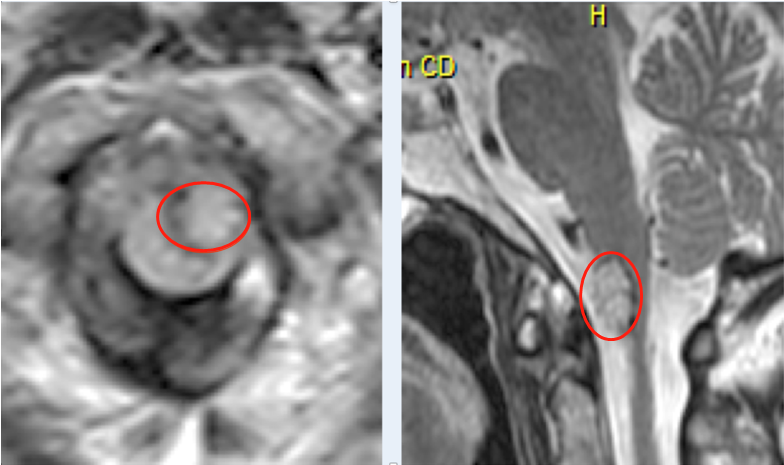
胶质母细胞瘤是星形细胞肿瘤中恶性程度较高的胶质瘤。肿瘤位于皮质下,多数生长于幕上大脑半球各处。呈浸润性生长,常侵犯几个脑叶,并侵犯深部结构,还可经胼胝体波及对侧大脑半球。发生部位以额叶较多见。
胶质母细胞瘤临床表现、病因
胶质母细胞瘤临床表现
胶质母细胞瘤生长速度快,70%~80%患者病程在3-6个月,病程超过1年者仅10%。病程较长者可能由恶性程度低的星形细胞瘤演变而来。由于肿瘤生长迅速,脑水肿广泛,颅内压增高症状明显,全部患者都有头痛、呕吐症状。视盘水肿有头痛、精神改变、肢体无力、呕吐、意识障碍与言语障碍。肿瘤浸润性损害脑组织,造成一系列的局灶症状,患者有不同程度的偏瘫、偏身感觉障碍、失语和偏盲等。神经系统检查可发现偏瘫、脑神经损害、偏身感觉障碍与偏盲。
胶质母细胞瘤病因
GBM的已知危险因素很少。电离辐射暴露是一个强危险因素,也是目前已知的可能致病因素。GBM和遗传性过敏症、变态反应及其他免疫相关问题呈负相关,这一点已被确认,但是其具体原因尚不明确。此外,一些少见的基因综合症与GBM相关,如Li-Fraumeni syndrome和Lynch syndrome,但是仅占病例的1%。值得注意的是,目前没有证据支持手机的使用与胶质瘤的发生有关,但这一结论目前仍有争论,还需要进一步的研究。
胶质母细胞瘤神经影像学
肿瘤部位和大体特征由于间质明显增生,所以肿瘤边界清楚,瘤质地硬,常位于颞叶和顶叶皮质下。CT和MRI检查类似转移瘤。
胶质母细胞瘤预后
胶质母细胞瘤是一种高度恶性的肿瘤,由于病变部位不同,一般病程较短,术后加以化疗为主要治疗手段,但是预后较差,一般生存期为6月到1年,影响预后的因素包括:坏死、临床评估、年龄、KI-67增生指数、遗传分子因素。
组织病理及分型
如同其他胶质瘤,GBM也被认为起源于神经胶质前体细胞。2016版WHO CNS肿瘤分类重新构建了胶质瘤的分型,将分子表型整合组织病理作为诊断标准。对于GBM诊断来说,引入IDH突变状态,分为:胶质母细胞瘤,IDH野生型和胶质母细胞瘤,IDH突变型。胶质母细胞瘤,NOS作为没进行IDH状态评估的情况补充。
组织学形态上,两种GBM亚型都存在高级别星形细胞瘤的特征,有微血管增生、局灶坏死(图1)。在IDH野生型GBM中,还存在一些不同的组织学亚型。巨细胞胶质母细胞瘤含有大的、多形性、多核巨细胞。胶质肉瘤可见高级别恶性星形细胞瘤特征和肉瘤样间质化生。上皮样胶质母细胞瘤是一类新认定的亚型,肿瘤细胞具有的上皮样形态,近半数出现BRAF V600E突变。尽管如此分型,但是目前并没有根据组织学亚型调整治疗建议。GBM和胶质肉瘤的经典MRI如图1。巨细胞胶质母细胞瘤及上皮样胶质母细胞瘤没有可靠的影像学特征进行鉴别。
IDH野生型GBM对应临床定义的原发GBM,也就是初发,没有既往确认的前驱病变。这一亚型占GBM的多数,近90%,常见于老年患者,临床进展恶化快。相反的,IDH突变型GBM或继发性GBM多起源于原有的弥漫星形胶质瘤或间变性星形胶质瘤,这一亚型约占10%,常见于年轻患者,平均发病年龄为44岁,预后相对较好。
除了IDH突变状态,在这两个亚型之间还有一些其他的基因表型差异(表2)。比如IDH野生型GBM中常有EGFR扩增、TERT启动子突变、PTEN缺失。MGMT启动子甲基化在IDH野生型GBM中占30-50%,可能提示较好的预后和对烷化剂化疗如TMZ的反应良好。IDH突变型GBM由低级别星形细胞瘤进展而来,伴有ATRX、TP53突变。CpG岛超甲基化现象在IDH突变型GBM可见,启动子甲基化在大量位点可见,这种类型肿瘤的预后可能较好。
2016版WHO 诊断指南中还增加了一种新的WHOIV级胶质瘤,H3F3A或HIST1H3B/CK27M(H3-K27M)突变,弥漫中线胶质瘤。这类肿瘤主要见于儿童及年轻人,预后不良。这类肿瘤既往可能也被归类为胶质母细胞瘤。
胶质母细胞瘤发病率及死亡率
2011-2015的注册数据显示在美国,GBM年龄修正平均年发病率为3.21/100000。年龄、性别影响发病率。诊断时的平均发病年龄为65岁,较高峰见于75-84岁。男性比女性多见,男:女=1.58,年龄修正后发病率分别为4/100000和2.53/100000。种群方面,非拉美裔白人(non-Hispanic whites)较高,美洲印安或阿拉斯加土著(American Indians or Alaska Natives)较低,发病率约下降40%。来看,GBM发病率在北美、澳洲、西欧、北欧发病率较高。美国的发病率为9.23/100000。
以上就是“胶质母细胞瘤临床表现、病因”的全部内容。
- 文章标题:胶质母细胞瘤临床表现、病因
- 更新时间:2021-08-26 16:56:37

 400-029-0925
400-029-0925