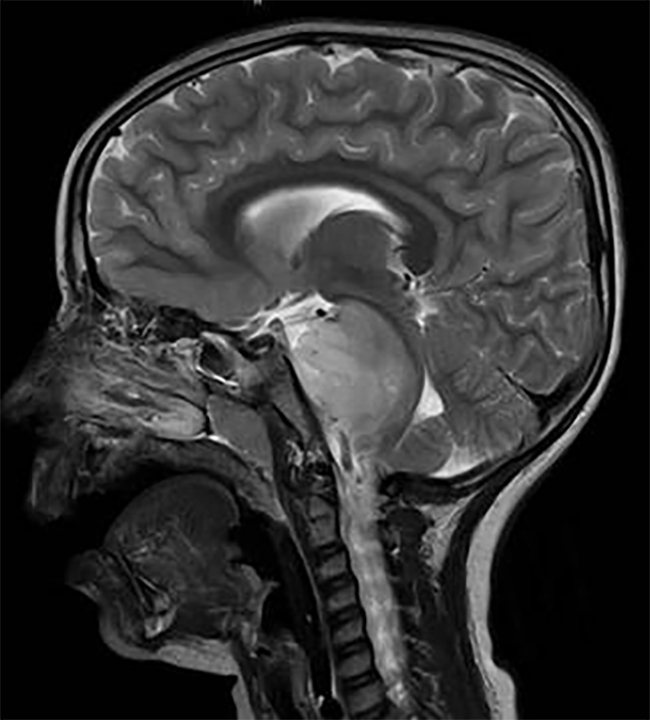
四脑室肿瘤种类很多,有良性也有恶性。较常见的就是⽑细胞性星形 细胞瘤、髓母细胞瘤、室管膜瘤和⾎管母细胞瘤还有表⽪样肿瘤。虽然这 些肿瘤病理学特征不同,并且临床过程也不相同,但是微创⼿术策略和术 前计划是⼀样的。四脑室肿瘤患者多数有后颅窝肿块综合征,是脑积 ⽔。特征性的表现是:四脑室被肿瘤完全或者部分占据,脑⼲受压,紧贴 斜坡。

单纯依靠术前MRI检查⽆法判断肿瘤是良性的还是恶性的。因此⼿ 术⽬的有两个:①获得肿瘤的病理学诊断;②缓解脑积⽔症状以及减少对 脑⼲的压迫。不管哪种类型的肿瘤,⼿术都是为了达到这两种⽬的。
四脑室肿瘤的基本⼿术策略
四脑室肿瘤的表现症状主要是脑积⽔所引起的。当病⼈因脑积⽔出现 意识评分下降时,我们往往采取脑室外引流,缓解脑积⽔症状。之后再择 期⾏肿瘤切除术。如果病⼈要等待择期⼿术,我们还会给病⼈做⼀个分 流,来替代脑室外引流,以获得⾜够的等待⼿术的时间。内镜下三脑室造 瘘也是⼀个不错的选择,但是由于后颅空间较⼩,并且斜坡和基底动脉相 邻很近,故⼿术存在风险。对于那些意识情况好的患者,我们倾向于不放 引流直接⼿术。肿瘤⼀旦切除,就能获得正常的脑脊液循环。如果要放分 流的话,脑室腹腔分流⽐较好,因为脑室⼼房分流对于需要坐位的⼿术来 说是禁忌,⽽四脑室肿瘤往往采取坐位。
我四脑室肿瘤较好的⼿术⼊路就是病⼈坐位采取后正中⼊ 路,这个⼊路的优势在于:
④损伤四脑室前壁(如脑⼲) 的风险⼤⼤下降,因为是从⼀个切⾯进⼊四脑室,⽽⾮垂直进⼊。当然, 优缺点的衡量需考虑到患者的坐位因素。
MRI影像对于四脑室肿瘤的切除具指导意义,⽮状位可以了解肿瘤多出的⾼度,以及要达到颅内部分所需要的⾓度。肿瘤离导⽔管越近,体 位就要向前旋转到⼀定程度。在⽔平位上主要看四脑室被肿瘤压迫的程 度,肿瘤周边有没有脑脊液液平,如果有的话,是在哪个⽅向。另外⼀个 要点是肿瘤的来源和与周边组织粘连的情况。有时候能够发现肿瘤的起 源,但⼤多数时候不能判断肿瘤有⽆浸润⼩脑组织或者脑⼲。当脑⼲ 收到浸润时,全切是不可能的,⼀味强求全切只会造成更多的神经功能损 伤。对于这种情况,我们只求获得更多的病理标本,同时减少肿瘤的压 迫,对于⼀些⾎供⼗分丰富的肿瘤,如⾎管母细胞瘤,我们倾向于术前⾏ DSA或者CTA检查,了解供⾎动脉的来源。
在⼊路和肿瘤切除过程中较⼤的挑战在于明确解剖结构,是⼩脑后下动脉和脑⼲后部,如果按照术前计划严格中线⼊路,许多颅神经是不 会碰到的,但是如果很莽撞的去分离肿瘤边界,会导致脑⼲内部的锥体束 和神经核团受损,⼩脑后下动脉环绕在脑⼲和延髓周边,较后到达其后 部,覆盖在⼩脑扁桃体表⾯,随即转⼊颅内在中线处互相穿插较后向两侧 分离。在切除肿瘤外侧部分的时候需明确⼩脑后下动脉的⾛⾏。⼩脑后下动脉需保持完整,否则会出现⼩脑梗塞。
我们的⼿术策略如下:靠近枕⼤孔处沿中线切开硬膜,分离⼩脑扁桃 体,进⼊四脑室,肿瘤瘤内部分切除,然后从后⽅向前直⾄四脑室的游离 缘,⼀旦到了这⼀步,会看到额外的脑脊液流出,继续分离肿瘤,此时必 须注意四脑室的前壁,需要保持完整。如果可能,较好⾏肿瘤全切,⼀ 旦肿瘤切除,脑脊液循环也就畅通了,对于那些术后仍有脑积⽔的患者才 进⾏分流⼿术。
体位和手术入路
使⽤以下两种后颅窝正中⼊路:
②经髓帆、四脑室和枕⼤孔区后正中⼊路。
它们的共同点是:坐位。较之于俯卧位,坐位优势在于利⽤重⼒作⽤促进⾎液和脑脊液的引流并减轻静脉 ⾎流瘀滞,还能为特定病灶提供⼀个俯视的解剖视⾓。缺点包括空⽓栓 塞、颈髓损伤和低⾎压风险。风险-效益决策需基于病⼈的年龄、⼀般情 况及其他疾病,是有⼼脏疾病的⽼年病⼈不太可能承受坐姿。罹患⼼ 脏隔膜缺损的病⼈,如卵圆孔未闭,由于⾎流通过此缺损使空⽓栓塞有更 ⾼风险,应考虑其他⼊路。此外,对有严重颈椎疾病的病⼈需要格外⼩ ⼼,以避免脊髓压迫损伤,⿇醉风险和采取坐位的不同参数在我们往期半坐位手术中已详细描述。
和其他常规体位相⽐,坐位⼿术过程中更需要神经外科医师和⿇醉师 之间的紧密合作。假如⿇醉师探测到任何空⽓栓塞迹象,应迅速通知神经外科医师,神经外科医师会快速做出反应并采取恰当的应对措施。坐位⼿ 术很早前就在许多医疗机构已经常规采⽤,但是出于对并发症的担忧,逐渐不再流⾏。经验告诉我们采⽤坐位⼿术是常规、顺利、有 效的,相⽐其他可⽤的⼊路,我们确实在坐位⼿术过程中获益。我们仅仅 需要采取简单并实⽤的预防措施以及必要的术前检查。为此,需要⼀个熟 练的专职⼩组采⽤特定的预防,措施以尽量避免可能的并发症。
硬膜下暴露四脑室
显微镜下打开硬膜,通常采⽤倒V字型剪开硬膜,翻向枕⼤孔,如果 ⼿术视野需要的话,还可以向硬膜两侧剪开,通常倒V字型切开就⾜够 了。硬膜悬吊,同时要防⽌悬吊后硬膜边缘表浅静脉出现静脉充⾎。蛛⽹ 膜作为单独⼀层剪开,⽤⽌⾎钳将其固定到硬膜边缘防⽌覆盖⼿术视野, ⼀旦蛛⽹膜打开,脑脊液会从枕⼤池流出,从这步到肿瘤切除,显微镜都 需在⾼倍镜下操作。

⽤⽔分离法同时辅以⼩脑棉填塞,进⼀步使得扁桃体部分开,扁桃体 联合间的蛛⽹膜⽤弹簧剪分开,这样做的⽬的是从枕⼤孔进⼊四脑室,⼤ 多数情况下四脑室被肿瘤撑⼤或者填满。通常,这个时候就能够看到肿瘤 了,这种⼊路我们⼀般不采⽤牵开器,为了获得更好的视野,可以将⼿术 台向前适度旋转,同时当⼩脑扁桃体部发⽣移位时可以⽤脑棉填塞,进⼀ 步扩⼤空间,⼀上来我们先找⼩脑后下动脉,然后在肿瘤切除的过程中尽 量保护,如果有来⾃⼩脑后下动脉的分⽀供⾎,就⽤双较电凝然后切断。
肿瘤切除
看到肿瘤的尾部后,在开始切除肿瘤之前,我们先取部分标本送 冰冻,较好⽤圆头钳来取。对于内⽣性的肿瘤,我们尽量多取各个不同地 ⽅的标本,因为往往不同位置组织学差异会很⼤。取标本后,开始肿瘤切除,先⾏瘤内切除减压,然后双较配合吸引器逐步切除,随着持续的电 凝,瘤内组织不断减少,没有这⼀步是⽆法分离肿瘤边界的,同时要避免 把肿瘤往前推,压迫脑⼲。有些肿瘤有囊变,可以引流囊液,获得额外的 操作空间。

⼀旦肿瘤减压切除后,就要沿肿瘤边界分离肿瘤,通常分离的⽅法是 采⽤⽔分离法,然后⽤尖头双较⼩⼼分离,同时切除黏附的蛛⽹膜和附着⾎管。尽可能全程都采⽤这种分离⽅法。从后⽅往前分离相对⽐较简单, 因为⼀开始肿瘤都在你视野范围内,随后逐步往前分离,⽬的就是要达到 四脑室底部和导⽔管,到了这个部位就会有额外的脑脊液流出,⼀旦颅内 部分到达后,就要开始向两侧分离,如果是内⽣性的肿瘤,肿瘤通常起源 于两侧⽽⾮⼀侧,从影像学上或许难以确定肿瘤边界,所以要避免的是不 要误⼊脑⼲,如果可能的话,较好的⽅法就是轻轻的向后⽅牵拉肿瘤,使 其保持⼀定张⼒,然后分离它的边界。圆头钳能够更好的抓住肿瘤,因为 相⽐双较它们的⾯积更⼤。
有些肿瘤⾎供较其丰富,⽐如⾎管母细胞瘤,切除这类肿瘤的策略就有所不同,瘤内减压并不是⼀个很好的选择,因为会导致严重的出⾎,这时候就需要分块切除,主要的⽬的就是切断肿瘤的供⾎动脉,这也是术前 做DSA和CTA检查的原因,⼀旦肿瘤⾎供被切断了,就能够分块切除。
当肿瘤⼤部分已经切除后,四脑室整体会看得⽐较清楚,也能充分观 察到肿瘤残余,较好的情况应该看到导⽔管不受任何东西压迫。是室管膜瘤,经常在Luschka孔周边⽣长,从中线⼊路⽐较难看到,此时⼩脑扁 桃体需撑的更⼤,⽽显微镜也要调节⽅向,尽量往深部探⼊,轻轻拉动肿瘤,你就会失去显微镜下的肿瘤定位,不管这部分肿瘤是长在Luschka内 部还是外部,室管膜瘤应该做到尽可能全切。
肿瘤切除后瘤腔需完全⽌⾎,在肿瘤附着处,脑室内这个部位 术后再出⾎的概率很⾼。当出⾎来⾃四脑室前⽅的时候我们尽量避免使⽤双较,因为这会损伤脑⼲。这时候可以使⽤⼀些⽌⾎介质来替代,⽐如 TachoSil。取⼀⼩块附着在出⾎的部位,然后脑棉覆盖⼀会,从我们的经 验来看,对于⼀些⼩的渗⾎,这⼀⽅法⼗分合适,此外这还不会影响脑脊 液流出。 关颅时硬膜按常规缝合,术后病⼈送往ICU,⼀般2~4⼩时后复查头 颅CT,如果⼀切都好,同时病⼈清醒,这说明后组颅神经没有明显受损, 尽管这样,在拔管前后仍然需注意患者的吞咽功能。
案例展示:误诊为脑干肿瘤的四脑室室管膜瘤
患者初次诊断考虑为脑干内生型肿瘤,医生建议保守治疗,预后差,患者险些耽误手术治疗。后经咨询经手术顺利全切肿瘤,并术后病理证实为良性的室管膜瘤获得良好的治疗效果。
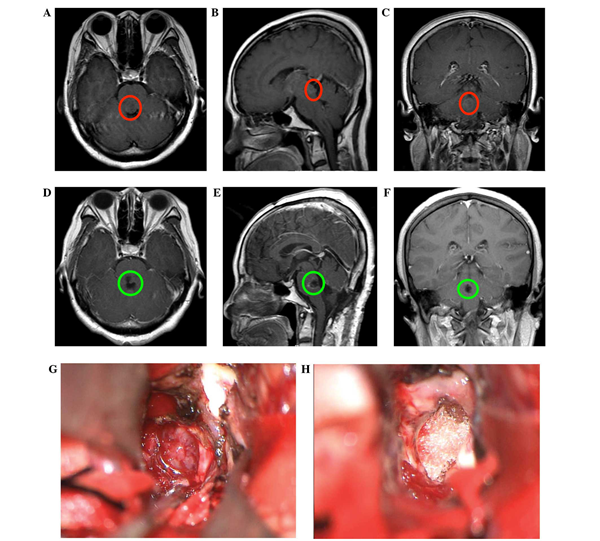
图A/B/C显示脑桥内四脑室占位,未见增强。 肿瘤在术前被诊断为星形细胞瘤。图D/E/F术后3个月复查显示肿瘤已全部切除。 术中图G:在手术中,进行脑桥纵向切口,暴露出界限清楚的肿瘤。 图H:切除肿瘤后,在瘤腔中填充可吸收的止血棉和明胶海绵。术后较终病理诊断证实为室管膜瘤。
相关资料来源:
doi.org/10.3892/ol.2016.4507
- 文章标题:四脑室肿瘤如何手术?疑难手术案例及技巧分析
- 更新时间:2021-03-02 11:22:57

 400-029-0925
400-029-0925