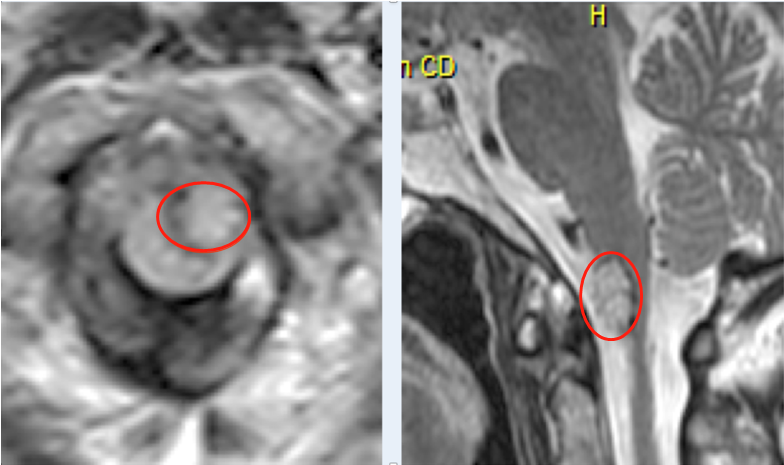
胶质母细胞瘤(GBM)是颅脑常见的恶性胶质瘤,其在基因分子水平诊断上分两种,分为IDH野生型和IDH突变型,IDH突变即为为异柠檬酸脱氢酶突变,是在这种肿瘤中发现的较重要的遗传改变之一。该文主要着重在IDH野生型胶质母细胞瘤的介绍。
胶质母细胞瘤经典问答
IDH野生型胶质母细胞瘤是全部星形细胞瘤中常见和较恶性的,WHO Grade IV,占GBM的95%以上。IDH野生型GBM有时也被称为“IDH野生型原发性胶质母细胞瘤”,以区别于IDH突变型GBM,后者是由低级IDH突变型星形细胞瘤引起的。
胶质母细胞瘤发病特点
IDH野生型GBM是假定的新生病变,没有可识别的低级前体肿瘤。但是,许多IDH野生型GBM的特征性遗传改变(例如TERT启动子突变,EGFR和PTEN突变,10p和10q染色体丢失等)也存在于大多数II级和III级野生动物中。类型的星形细胞瘤,提示它们可能构成同一疾病的连续体。三种遗传性癌症综合征,即1型神经纤维瘤病(NF1),Li-Fraumeni和Turcot综合征,显示出发展为IDH野生型GBM的倾向性增强。
与IDH突变型GBM(参见下文)相反,IDH野生型GBM分布在整个大脑半球。它们较先侵犯皮层下和脑室深部白质,它们容易散布在紧凑的区域,如胼胝体体和皮质脊髓区域。胼胝体对称累及是常见的,即所谓的“蝴蝶神经胶质瘤”模式(图1)。IDH野生型GBM的大小差异很大,由于它们可以迅速沿着致密的白质区域广泛传播,因此在初诊时较多有20%表现为多灶性病变。在多灶性GBM中,有2-5%是的同步性,独自发展的肿瘤。
胶质母细胞瘤肿瘤微观和大体特点
常见的外观是围绕中央坏死核的红灰色肿瘤“外皮”,占位效应和肿瘤周围水肿明显。血管增多和肿瘤内出血是常见的。坏死和微血管增生是GBM的组织学标志,将它们与间变性星形细胞瘤区分开来。各种肿瘤细胞包含GBM。多形性原纤维星形细胞,双核细胞,双较乏力但有丝分裂活性的小细胞(包括“小胶质细胞”)和奇异的多核巨细胞都是常见的特征。GBM通常具有高增殖指数(MIB-1),几乎总是>10%。
胶质母细胞瘤影像学
多数IDH野生型GBM表现出围绕坏死重要的厚、不规则、增强的“外皮”肿瘤。在少数情况下,不存在优势质量。相反,肿瘤扩散到整个脑白质。T2/FLAIR扫描上的融合性和斑块状白质高信号模拟小血管疾病。甚至更少见的变体是“原发性弥漫性软脑膜胶质瘤病”。
胶质母细胞瘤CT检查特点
大多数IDH野生型GBM在NECT(图2A)上显示出低密度的中央肿块,周围有等密度到中等密度的边缘。出血很常见,但钙化很少。明显的肿块效应和明显的低密度肿瘤周围水肿是典型的辅助发现。CECT显示出强大但异质的不规则边缘增强(图2B)。高血管性GBM中的突出血管被视为邻近肿块的线性增强灶。
胶质母细胞瘤MR影像特点
T1WI显示边缘质量差,信号强度混合。亚急性出血是常见的。T2/FLAIR表现为异质性高信号,肿瘤边缘不清楚,血管广泛水肿。可能会出现坏死,囊肿,转化为各个阶段的出血,体液/碎片水平以及大量新生血管引起的“血流空洞”。T2成像通常显示易感伪影的病灶。
T1 C+显示围绕坏死肿瘤中央非增强重要的强烈但不规则的环增强(17-44)。主要肿块外的结节状,点状或斑片状增强灶代表肿瘤向邻近结构的扩展。在标准成像序列上,肿瘤细胞的小灶始终存在,远远超出了任何明显的增强或水肿区域。
胶质母细胞瘤治疗和预后
胶质母细胞瘤好转症状、延长生存期的较合适方式是手术切除肿瘤,术后辅以放化疗治疗,尽管如此,这些患者的总体生存率还是不乐观。GBM是一种无情的进行性疾病,IDH野生型GBM患者的平均生存期不到1年,目前几乎全部研究结果均表示,年轻患者具有更好的生存期,大规模的人群研究也提示,年龄是较的预后因素。此外,MGMT启动子甲基化是对烷基化剂反应的强烈评估指标,可以增加化疗敏感性,有助提高预后。
胶质母细胞瘤病因
GBM的已知危险因素很少。电离辐射暴露是一个强危险因素,也是目前已知的可能致病因素。GBM和遗传性过敏症、变态反应及其他免疫相关问题呈负相关,这一点已被确认,但是其具体原因尚不明确。此外,一些少见的基因综合症与GBM相关,如Li-Fraumeni syndrome和Lynch syndrome,但是仅占病例的1%。值得注意的是,目前没有证据支持手机的使用与胶质瘤的发生有关,但这一结论目前仍有争论,还需要进一步的研究。
胶质母细胞瘤预后
胶质母细胞瘤是一种高度恶性的肿瘤,由于病变部位不同,一般病程较短,术后加以化疗为主要治疗手段,但是预后较差,一般生存期为6月到1年,影响预后的因素包括:坏死、临床评估、年龄、KI-67增生指数、遗传分子因素。
胶质母细胞瘤发病率及死亡率
2011-2015的注册数据显示在美国,GBM年龄修正平均年发病率为3.21/100000。年龄、性别影响发病率。诊断时的平均发病年龄为65岁,较高峰见于75-84岁。男性比女性多见,男:女=1.58,年龄修正后发病率分别为4/100000和2.53/100000。种群方面,非拉美裔白人(non-Hispanic whites)较高,美洲印安或阿拉斯加土著(American Indians or Alaska Natives)较低,发病率约下降40%。来看,GBM发病率在北美、澳洲、西欧、北欧发病率较高。美国的发病率为9.23/100000。
胶质母细胞瘤组织病理及分型
如同其他胶质瘤,GBM也被认为起源于神经胶质前体细胞。2016版WHO CNS肿瘤分类重新构建了胶质瘤的分型,将分子表型整合组织病理作为诊断标准。对于GBM诊断来说,引入IDH突变状态,分为:胶质母细胞瘤,IDH野生型和胶质母细胞瘤,IDH突变型。胶质母细胞瘤,NOS作为没进行IDH状态评估的情况补充。
组织学形态上,两种GBM亚型都存在高级别星形细胞瘤的特征,有微血管增生、局灶坏死(图1)。在IDH野生型GBM中,还存在一些不同的组织学亚型。巨细胞胶质母细胞瘤含有大的、多形性、多核巨细胞。胶质肉瘤可见高级别恶性星形细胞瘤特征和肉瘤样间质化生。上皮样胶质母细胞瘤是一类新认定的亚型,肿瘤细胞具有的上皮样形态,近半数出现BRAF V600E突变。尽管如此分型,但是目前并没有根据组织学亚型调整治疗建议。GBM和胶质肉瘤的经典MRI如图1。巨细胞胶质母细胞瘤及上皮样胶质母细胞瘤没有可靠的影像学特征进行鉴别。
IDH野生型GBM对应临床定义的原发GBM,也就是初发,没有既往确认的前驱病变。这一亚型占GBM的多数,近90%,常见于老年患者,临床进展恶化快。相反的,IDH突变型GBM或继发性GBM多起源于原有的弥漫星形胶质瘤或间变性星形胶质瘤,这一亚型约占10%,常见于年轻患者,平均发病年龄为44岁,预后相对较好。
除了IDH突变状态,在这两个亚型之间还有一些其他的基因表型差异(表2)。比如IDH野生型GBM中常有EGFR扩增、TERT启动子突变、PTEN缺失。MGMT启动子甲基化在IDH野生型GBM中占30-50%,可能提示较好的预后和对烷化剂化疗如TMZ的反应良好。IDH突变型GBM由低级别星形细胞瘤进展而来,伴有ATRX、TP53突变。CpG岛超甲基化现象在IDH突变型GBM可见,启动子甲基化在大量位点可见,这种类型肿瘤的预后可能较好。
2016版WHO 诊断指南中还增加了一种新的WHOIV级胶质瘤,H3F3A或HIST1H3B/CK27M(H3-K27M)突变,弥漫中线胶质瘤。这类肿瘤主要见于儿童及年轻人,预后不良。这类肿瘤既往可能也被归类为胶质母细胞瘤。
胶质母细胞瘤发病率
巨细胞胶质母细胞瘤是一个少见亚型,占全部脑肿瘤的不足1%,占胶质母细胞瘤的5%。
胶质母细胞瘤高发年龄和性别
患者以中老年居多,巨细胞胶质母细胞瘤平均发病年龄42岁,但年龄跨度比弥漫型星形细胞瘤大,儿童也可发病。男女之比为1:1.6。其表现与常见的多形性胶质母细胞瘤有的区别,术前诊断存在困难。
胶质母细胞瘤遗传学
巨细胞胶质母细胞瘤以经常出现TP53突变(75%~90%)和PTEN突变(33%)为特征,但没有EGFR扩增/过表达和纯合性p16缺失。这些结果表明巨细胞胶质母细胞瘤有双重特性,它与原发性胶质母细胞瘤在临床病史较短、没有低度恶性前体病变和高PTEN突变率上相似。与低级别星形细胞瘤进展而来的继发性胶质母细胞瘤相比,都有发病年龄较轻和高TP53突变率的特点。
胶质母细胞瘤组织病理学
肿瘤含有较多的巨怪形多核巨细胞、小纺锤状的合体细胞和含量不等的网状纤维。巨细胞形态奇异,直径>500μm,核可20多个,常为角状,并含有明显的核仁,有时可见胞质内包涵体、假栅栏状坏死和大片缺血性坏死。非典型核分裂常见,但增生率同胶质母细胞瘤。GFAP表达差异很大,偶见血管周围淋巴套,也可见肿瘤围绕血管分布,形成不典型的假菊形团。TP53突变基因产物主要位于核内。
以上就是“胶质母细胞瘤经典问答”的全部内容。
- 文章标题:胶质母细胞瘤经典问答(二)
- 更新时间:2021-08-26 17:02:59

 400-029-0925
400-029-0925