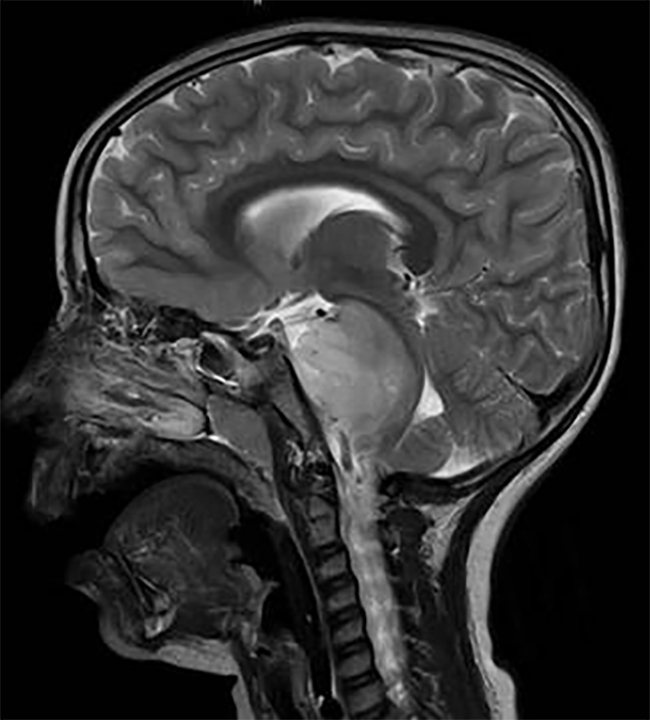
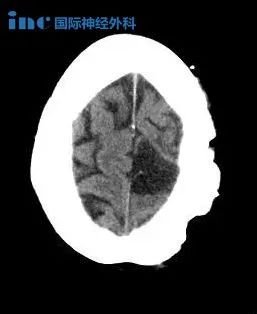
质子治疗室管膜瘤效果好吗?通过减少进入前颅结构(如耳蜗、脑下垂体和颞叶)的放射剂量,质子可以降低室管膜瘤患者的晚期毒性风险。室管膜瘤患者在接受放射治疗时通常很年轻,诊断时的平均年龄为5-6岁。麦克唐纳等人的一项研究强调了质子治疗的剂量学益处,该研究比较了17例后颅底室管膜瘤儿童的质子治疗和调强放疗(IMRT)计划的剂量分布。通过质子疗法可以观察到对整个大脑和颞叶的辐射剂量减少。尽管调强放疗的耳蜗剂量也很低(平均剂量3 Gy),但质子对耳蜗的放射剂量基本上没有受到任何影响。
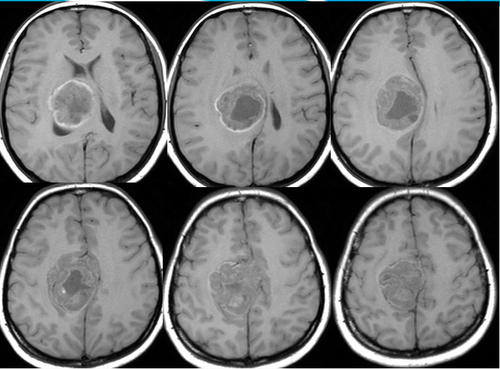
MacDonald等人也发表了大量的质子治疗室管膜瘤的临床系列,包括2000年至2011年在MGH治疗的70例局限性疾病的儿童。中位年龄为38个月,大多数患者有幕下疾病(73%)、经典组织学(53%)和全切除(GTR)(66%)。质子的中位剂量为55.8 Gy(相对生物学效应[RBE]),57%的患者接受的剂量高于54 Gy(RBE)。在46个月的中位随访中,3年的局部控制(LC)、无进展生存期(PFS)和总生存期(OS)分别为83%、76%和95%。甲状腺功能减退的患者占1/32(3%),生长激素缺乏的患者占2/25(8%)。生长激素缺乏的比率可能与脑积水混淆,在治疗前有54%的患者存在脑积水。耳蜗中位剂量为7 Gy(RBE),但由于延伸至四脑室外侧孔,需要覆盖至或进入内耳道,剂量范围为0~54 Gy(RBE)。有2/23(9%)可评估的患者因辐射而导致听力损失,两者均因疾病提前扩展而接受了几乎全剂量的耳蜗治疗。队列中无脑干坏死病例。
Ares等在文献的基础上发表了在Paul Scherer研究所用质子治疗50例颅内室管膜瘤的结果。中位年龄为31个月,中位辐射剂量为59.4 Gy(RBE),72%患有幕下疾病,66%接受全切除(GTR)。5年LC率和OS率分别为78%和84%,有残留疾病者和无残留疾病者的LC率分别为77%和91%。治疗后中枢性甲状腺功能减退和生长激素缺乏的发生率均为6%。单侧听力丧失2例(4%)。一名患者死于致命的脑干坏死;该患者较初接受GTR和化疗治疗,复发后需要在放疗之前进行二次手术。二次手术因脑干梗塞和脑膜炎而复杂化。
Sato等人发表了他们对德克萨斯州儿童医院使用光子(38例)或质子(41例)放疗和MDACC治疗的79例室管膜瘤患者的回顾性分析。3年的PFS率在光子组为60%,在质子组为82%(P=0.031),两组之间的LC率没有差异(两组为86%)。全部失效都发生在高剂量区。接受质子治疗的患者更年轻(中位年龄,2.5岁对5.7岁;P=0.001),中位随访时间更短(2.6年比4.9年;P<0.0001)。质子组的GTR频率高于调强放疗IMRT组(93%比76%);P=0.043)。6例患者(光子组3例,质子组3例)出现症状并经影像学诊断为放射性坏死。
较近,Indelicato等人发表了179例非转移性II/III级室管膜瘤儿童使用质子治疗的结果。在平均3.2年的随访中,临床结果与3年LC和OS分别为85%和90%的光子序列相当。3年的PFS为76%。与其他系列相似,多因素分析发现次全切除与下段LC(67%比88%,P≤0.01)和PFS(59%比79%,P&<0.05)相关。有趣的是,男性也与较低的PFS(67%vs 87%,P<0.05)和OS(84%vs.99%,P<0.01)相关。10例患者出现症状性脑干毒性,经过精算的3年不良事件通用术语标准(CTCAE),2级+脑干毒性率为5.5%(95%CI:2.9-10.2),其中1例出现5级毒性。
这些质子系列的疾病结果似乎可与规模较大的光子组比较。Tensaouti等人评估了法国206名接受各种放射治疗的儿童颅内室管膜瘤患者,包括光子和质子治疗。在整个队列中,84例患者在平均53.8个月的随访中出现复发。有趣的是,该小组对90名接受剂量≥59.4 Gy的患者进行了二次效应或后遗症回顾,剂量学分析显示,根据脑干的较大剂量或平均剂量,后遗症发生率没有统计学上的差异。
哪里可以进行质子治疗?
INC合作的法国居里癌症研究所质子中心、日本国立癌症中心质子治疗中心、日本江户川医院等提供不同领域的专家紧密协作(包括成人/儿科肿瘤学家、神经外科专家、麻醉学家、临床医生和其他相关人士),为患者进行前沿、的质子治疗。当前在疫情防控的不同时期,法国居里癌症研究所质子中心可接诊国内患者,追求更高术后生活质量和更高生存率的国内患者可通过INC前往法国进行质子治疗。
- 文章标题:质子治疗室管膜瘤效果好吗?
- 更新时间:2020-06-30 14:06:52

 400-029-0925
400-029-0925