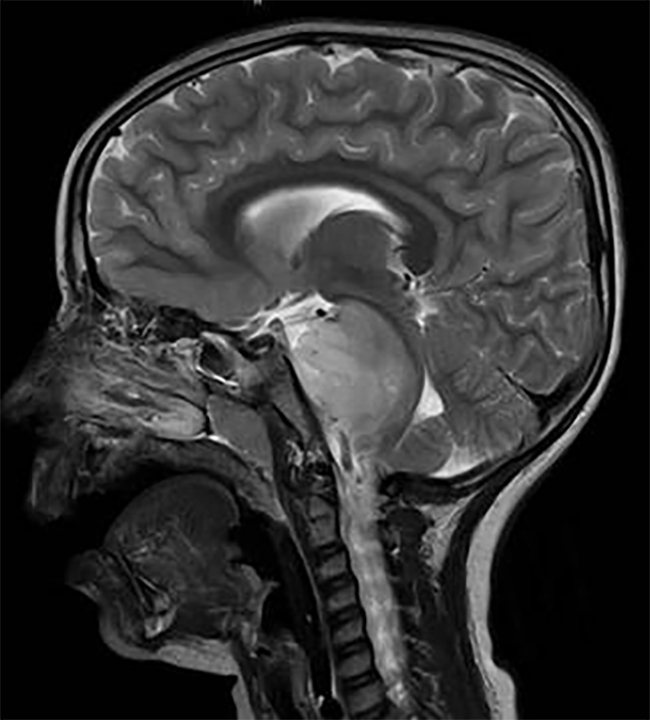
神经胶质瘤是小儿患者中常见的脑癌类型,约占全部儿童颅内肿瘤的50%。这是一个高度异质的人群,从良性的WHO组织病理学I级和II级到恶性的WHO III级和IV级,患者情况各有差异。病理组织学和位置是重要的预后因素,会影响手术干预的决策以及可能切除肿瘤的程度。INC旗下国际神经外科顾问团(WANG)的专家成员、国际神经外科学院前主席、儿童神经外科专家James T.Rutka教授曾发表论文就儿童胶质瘤的组织学、位置、手术策略及预后因素等进行了深入分析。

INC之加拿大James T.Rutka教授的论文
Rutka教授总结:在低级别神经胶质瘤中,外科手术全切仍然是较佳的选择。与成人相比,儿童高级神经胶质瘤(高级别胶质瘤)的治疗仍构成挑战。在非脑干高级别胶质瘤中,手术的目标往往是较大水平地顺利切除肿瘤,但这通常在弥漫性桥脑神经胶质瘤(DIPG)中不起作用。因此,在大多数高级别胶质瘤病例中,治疗方案还需更为个体化。对视神经胶质瘤患者的手术干预包括活检,STR或肿瘤全切。
常见类型与临床表现
儿童较常见的脑瘤是良性低级别胶质瘤(低级别胶质瘤),包括毛细胞星形细胞瘤(PA)和室管膜下巨细胞星形细胞瘤(二者均为WHO I级)和弥漫性星形细胞瘤(WHO II级)。WHO III级(例如间变性星形细胞瘤)和IV级(多形胶质母细胞瘤)的高级别神经胶质瘤(高级别胶质瘤)在儿童中少见。这些肿瘤与弥漫性桥脑神经胶质瘤(DIPG)一起构成全部小儿脑肿瘤的约20–25%。高级别胶质瘤在婴儿期很少见,但其发病率随年龄增加而增加,在青少年中较高。
小儿颅内神经胶质瘤患者的一般症状为易怒、发育不良和大头畸形等,其他体征通常与特定的肿瘤位置有关,例如皮质病变会导致患者癫痫发作,脑干病变的颅神经病变以及脑脊液(CSF)流动障碍会造成脑积水等。
低级别胶质瘤
低级别胶质瘤是一种异质性肿瘤,临床上多表现为无症状,经适当治疗后10年生存率可达80%。较常见的低级别胶质瘤是后颅窝星形细胞瘤(占全部中枢神经系统[CNS]肿瘤的15–25%)和大脑半球星形细胞瘤(占全部CNS肿瘤的10–15%)。低级别胶质瘤也会出现在中线结构(即丘脑,胼胝体,下丘脑和脑室区域)以及视神经通路附近或视神经通路内,占全部中枢神经系统肿瘤的10%至20%。根据临床表现和影像学表现,还有多达20%的脑干肿瘤被诊断为低级别胶质瘤。
PA是儿童年龄组中常见的神经胶质瘤,它主要发生在幼儿(中位年龄为4岁)中。PA在后颅窝、视神经通路、背侧分叶状、外生性脑干肿瘤中所占比重较大,在t1加权像上通常表现为低张力囊性肿块,实性部分增强明亮(图1)。
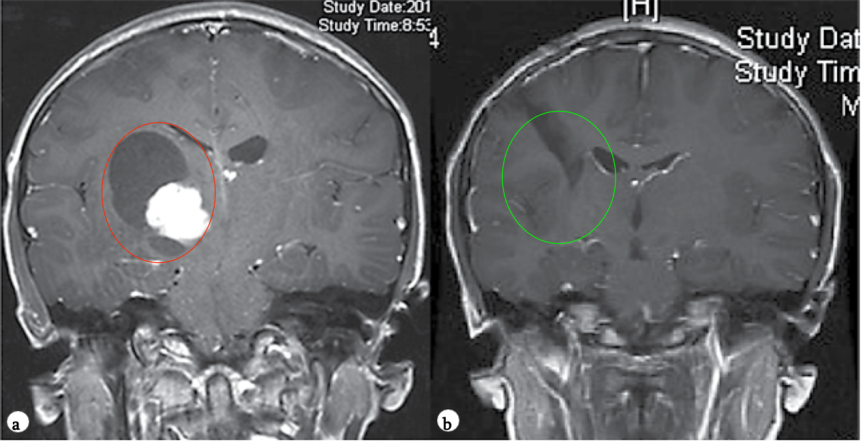
图1。术前(a)和术后(b)颅脑磁共振MR,术前MR显示右侧丘脑较大囊实性占位,胶质瘤可能,皮质脊髓束(负责人体肢体运动的神经传导束)受压,脑室扩大,术后MR显示肿瘤全切,脑组织复位,无脑出血、脑水肿等损伤。
低级别胶质瘤的神经外科切除术为病理诊断提供了组织,并为顺利地较大水平减轻肿瘤压迫提供了机会。对于大脑半球、小脑、局灶性和背侧外生性脑干、颈髓等部位的肿瘤、特别是对于WHO I级肿瘤而言,肿瘤全切是优选的治疗方法。通常可以沿清晰的肿瘤边界仔细解剖肿瘤团块,将PA从周围的大脑中完全切除。
低级别胶质瘤的切除范围(肿瘤切除程度)是临床预后的重要评估指标。肿瘤切除程度>95%时,5年和10年生存率从75%到100%不等。有研究显示:接受肿瘤全切治疗的低级别胶质瘤患者10年无进展生存期(PFS)为100%,而次全切(STR)后为67-81%。尽管可通过手术切除控肿瘤进展,但仍建议进行密切的术后临床和放射随访,以及时发现肿瘤可能的复发或进展。
视神经通路/下丘脑低级别胶质瘤
视神经通路/下丘脑胶质瘤是典型的低级别星形细胞瘤,可发生在视神经通路的任何位置,也可能累及下丘脑。它们相对少见,通常出现在儿童时期,其中20%-30%与1型神经纤维瘤病(NF1)有关。从惰性的毛细胞星形细胞瘤(PA)到更具攻击性的毛细胞粘液样星形细胞瘤(PMA),甚至是少见的侵袭性生长的高级别胶质瘤,视神经胶质瘤在生长潜力上往往会表现出相当大的差异。
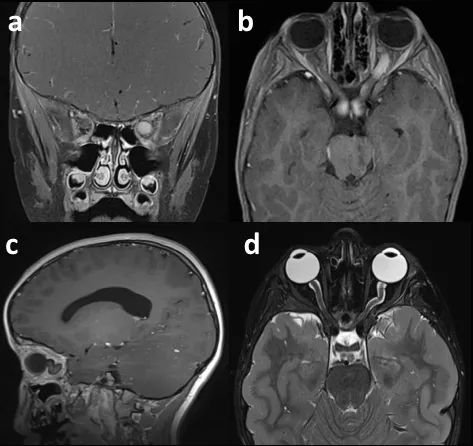
视神经胶质瘤
视路胶质瘤常见初始症状是视力障碍,如视力下降和视野缺损等症状。前部病变直接累及眼眶内视神经,使患者容易出现眼球突出,斜视和单眼视力缺陷。后部病变倾向于双侧视野受累,使眼球震颤和内分泌病变的发生率有所增加。视觉诱发电位(VEP)是一种有用的辅助手段,可以被用于评估幼童的视觉系统。一些患者还可能出现颅内压(ICP)升高的特征,通常继发于脑积水。21%的视神经交叉-下丘脑胶质瘤患者出现了间脑综合征,包括恶病质、脑白斑、眼球震颤和视觉通路缺陷等。
在前部视神经胶质瘤病变中进行手术的主要指征是为已经失明或视力较差的患者中处理眼球突出症。局限在视神经眶内和部分神经管内的视神经胶质瘤几乎可以通过手术被治愈。这些病变可通过视神经后方切至距视交叉3-5毫米,前切至眼球后,这些都可以通过单侧额下入路硬膜外通过磨除眶顶达到手术目的。
视路胶质瘤后部病变的手术更具挑战性。许多治疗该区域肿瘤的方法都已被描述过,包括额下、颞下、经胼胝体和前半球间入路。根据肿瘤的精确位置和外科医生的经验或偏好而做出选择。由于邻近的结构(视神经束、丘脑、下丘脑和脑干)较为脆弱,因此肿瘤全切略显激进。常见的手术目标是次全切肿瘤,当然手术目标也可能更为具体一些,比如对视神经通路或其他神经结构的减压,肿瘤囊肿的开窗,以及脑积水的处理。就后者来说,仅手术切除肿瘤可能还不够,还需要放置脑室-腹腔(VP)分流术。
手术后,需对患者进行监护。如果患者患有复发性或进行性病变,则还需进行抢救性手术、放疗(FRT)或临床试验化疗方案。还应在可获得的益处与潜在的治疗发病率之间仔细权衡。
脑干胶质瘤
脑干低级别胶质瘤是一组异质性肿瘤,可以根据解剖位置和临床行为进行分类。确定了三个主要类别:(1)中脑(顶盖或被盖);(2)桥脑(背部外生性,局灶性和DIPG);(3)颈髓肿瘤。在这些病变中,DIPG和某些局灶性脑桥脑干神经胶质瘤通常是恶性的。
●顶盖胶质瘤是一种病程为良性的惰性肿瘤。患者通常表现为颅内压升高,继发于梗阻性脑积水,原因是靠近或阻塞中脑导水管。直接切除肿瘤的情况很少,手术干预的主要指征是通过VP分流术或内镜下三脑室造口术治疗脑积水。大多数患有顶盖神经胶质瘤的患者术后会进行一系列神经影像学研究。如果出现肿瘤进展,则建议手术,化疗,FRT或立体定向放射外科手术(SRS)等方式治疗。
●被盖脑胶质瘤是中脑脑干神经胶质瘤,通常造成儿童局灶性单侧无力,上颅神经麻痹影响眼外肌。PA多发于此位置,并且可以通过经侧裂入路、经颞叶入路或经胼胝体半球间入路进行神经外科手术切除。如果无法手术全切,可辅以化疗和/或放疗继续治疗。
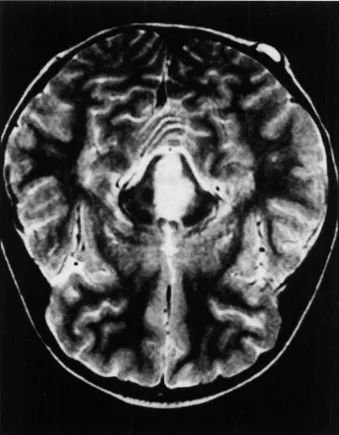
被盖胶质瘤
●背侧外生性脑桥胶质瘤起源于四脑室底的室管膜下胶质细胞,通常向阻力较小的方向生长,进入脑室腔和蛛网膜下池。小儿患者通常表现为眼外肌功能障碍,这是由于桥旁网状结构受累所致。这些良性病变通常在MRI上表现为相当大,可能类似小脑星形细胞瘤。然而,与小脑星形细胞瘤不同的是,背侧外生性桥脑胶质瘤在四脑室阻滞后直到病程很晚才产生脑积水。手术的目标应该是较大限度的切除肿瘤和较小手术并发症。为能更加顺利、完全地切除肿瘤,需在术中持续使用对运动、感觉和脑神经功能的神经生理监测。神经外科手术的另一个关键要点是不要超出四脑室的预期位置,以避免发生新的颅神经病和增加其他神经功能缺损的风险。神经外科手术切除后可根据需要使用化疗和FRT。
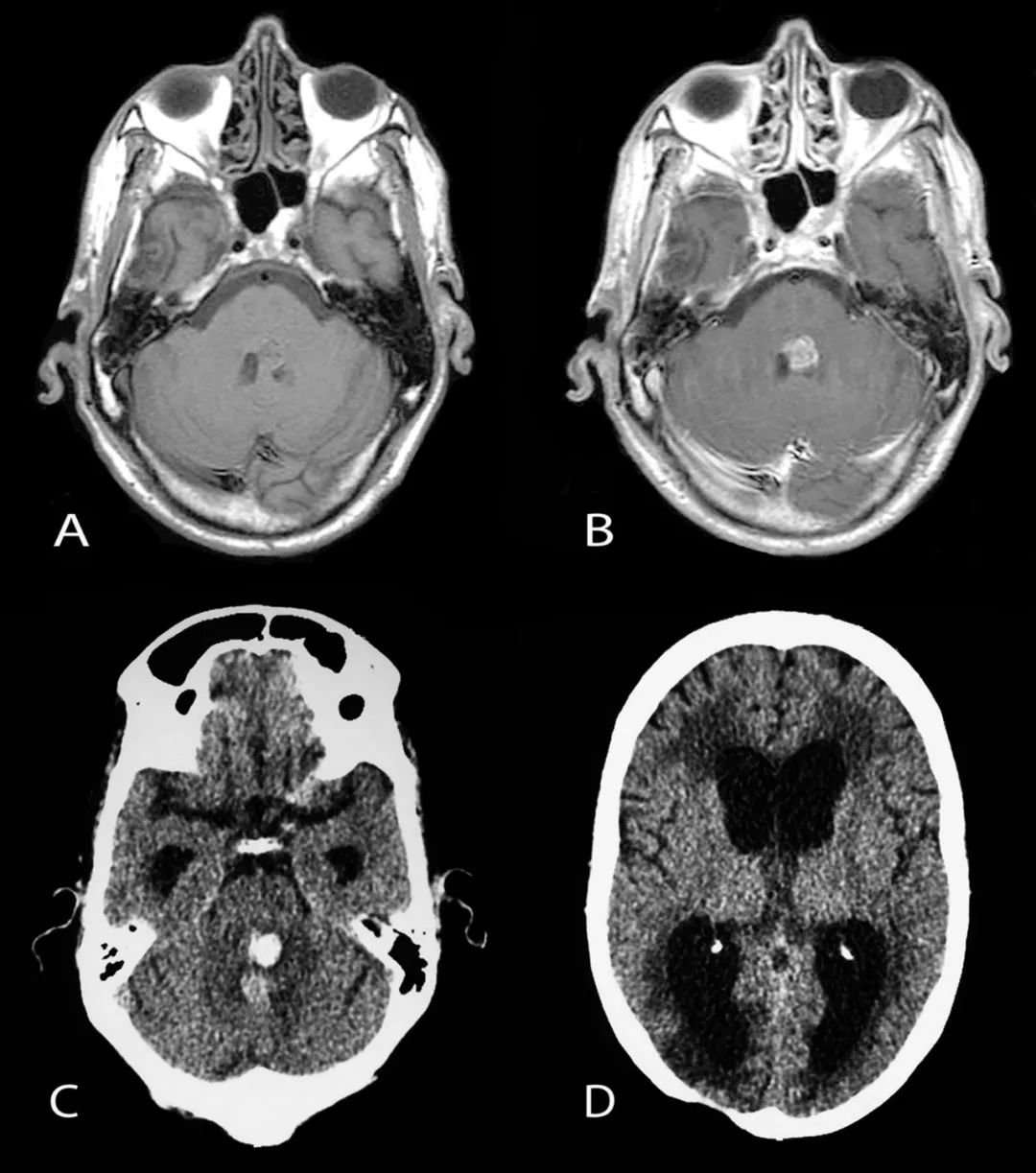
背侧外生性脑桥胶质瘤
●儿童颈髓胶质瘤典型表现为进行性共济失调、下颅神经功能障碍。神经外科切除术在患者管理中起着重要作用,但应在较高精度的显微神经外科手术设备和持续的术中神经生理学监测条件下进行,目的是达到较大限度的顺利切除病变。许多患者将需要术后化疗和/或FRT(图2)。此外,随着时间的推移,患有此类肿瘤的儿童可能需要某种形式的枕颈稳定。
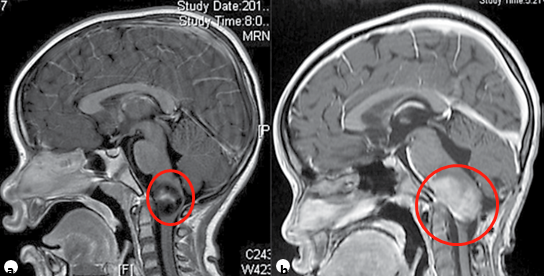
图2。一名7岁儿童浸润性颈髓肿瘤的矢状面造影后t1加权MRI(a)。活检和组织病理学诊断为低级别肿瘤,尽管使用化疗(b)和FRT来治疗控制肿瘤生长,但肿瘤仍在进展。
致痫性肿瘤
致痫性肿瘤主要属于胶质细胞和神经细胞混合成分的胶质细胞性肿瘤一类。这些少见的病变以癫痫发作为主要症状。手术切除后患者的预后较好。
●神经节神经胶质瘤(WHO I级)是较常见的致癫痫性肿瘤,尽管它仅占全部脑肿瘤的1-4%。它往往发生在具有长期癫痫病史的儿童和年轻人中,通常难以凭借药物控制。复杂的部分发作较为常见。尽管神经节胶质瘤倾向于出现在颞叶,但它可发生在神经轴的任何地方,包括颈髓连接处、松果体和鞍上区域。颞部外的位置与组织学异型性和间变性相关(间变性神经节胶质瘤;手术是这些肿瘤的主要治疗手段[见图3])。虽然有报道称有恶性变可能,但其通常是良性的。幕上神经节胶质瘤通常可以手术全切,因此这是可治愈的,也为80%的患者达成了Engel I型发作结局。为了进一步好转癫痫发作的控制,建议行脑损伤切除联合邻近颞部新皮质切除术,肿瘤全切的主要障碍是肿瘤的中线位置(如脑干),而其他限制因素包括分界差、靠近主皮层和浸润了重要结构。
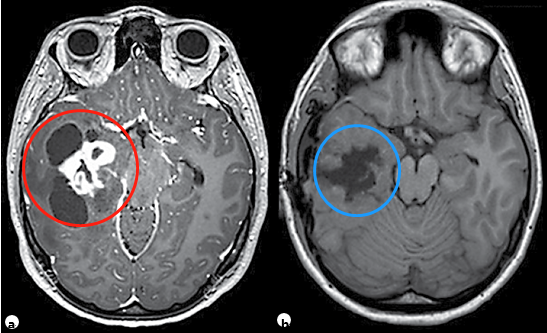
图3。11岁患儿,右颞部肿瘤多发囊肿并增强强化的实性瘤体部分,术前和术后轴位t1加权MRI对比,提示肿瘤被完全切除,病理诊断为神经节胶质瘤。
●DNET是二常见的胶质神经元肿瘤。典型的表现为一种皮质基底的幕上病变,易累及颞叶,并伴有慢性局灶性癫痫。通常在CT或MRI上既没有强化增强,也没有肿块效应或淋巴管周围水肿。凹凸病变可导致上覆骨呈扇形。20-30%的病例出现钙化。组织学上,DNET可能被误认为是少突胶质细胞瘤,因为前者含有类似少突胶质细胞的细胞。这些肿瘤的边界易被分辨,因此可以通过手术切除。部分切除的肿瘤进展率虽低,却可能与持续或复发的癫痫发作有关。对于进展性或复发性DNET,可以采用重复手术治疗,因此不需要辅助治疗。
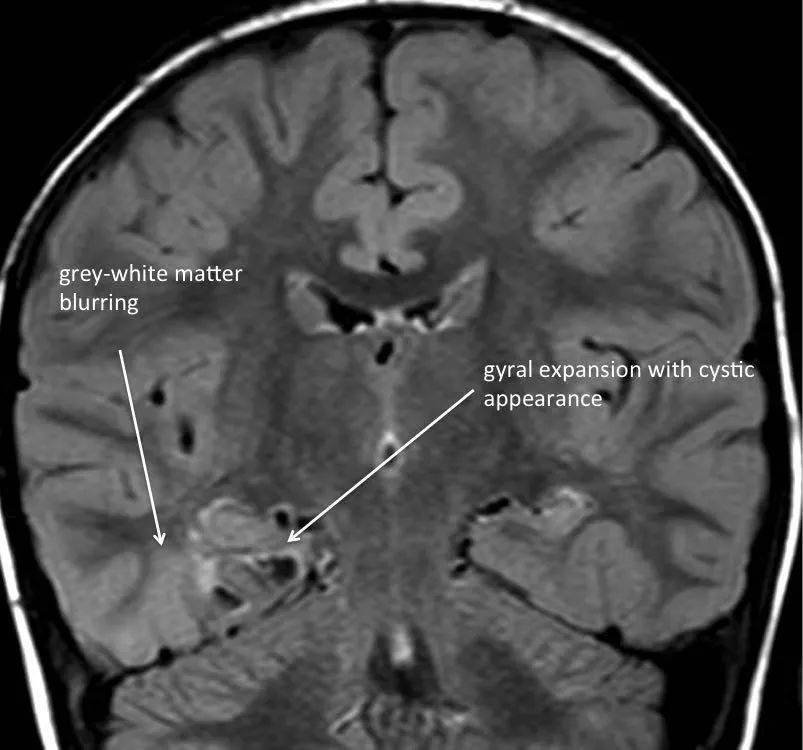
DNET
高级别胶质瘤
儿童期高级别胶质瘤的病因尚待确定,但已经确定了某些危险诱因,包括以前曾接受过放射线照射和存在某些遗传的家族性综合症,例如Li-Fraumeni,Turcot和NF1。儿童高级别胶质瘤的分子谱已被描述与成年人不同。非脑干(主要是幕上)和脑干(以DIPG为代表)病变的生物学行为、治疗和结果往往不同。然而,无论生发在哪里,这些边界不明确,高度浸润的肿瘤都较难治疗,这对任何儿童神经肿瘤学家都是一个的挑战。
患有高级别胶质瘤的儿童的症状与在良性肿瘤中发现的症状相似。然而,临床病程通常更为突然,有颅内压升高或局灶性神经功能障碍的快速进展体征。癫痫发作是一种少见的表现形式。由于瘤内出血,约5-10%的患者的病情会突然恶化。
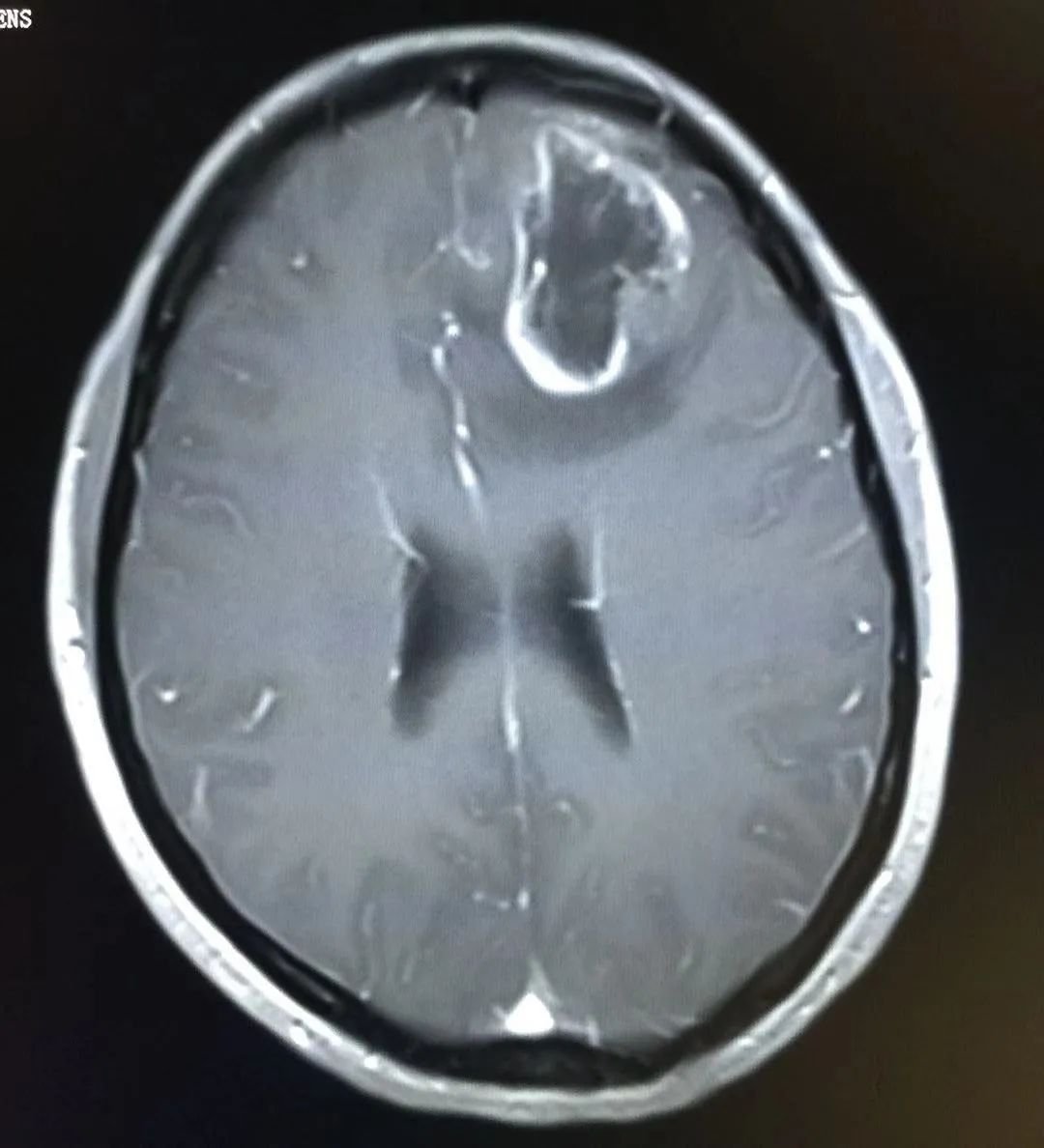
高级别胶质瘤
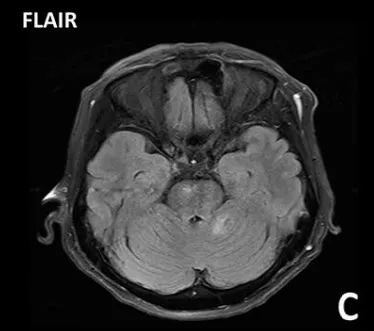
非脑干高级别胶质瘤的特征性MRI表现包括t1加权像低信号,t2加权像皮质和白质高信号(表现浸润性肿瘤和血管反应性水肿)和不规则增强。DIPG通常表现为大的扩张性脑干肿块,中心位于脑桥,占其三分之二。病变通常在T1上具有低强度或等强度信号,边缘模糊不清,在T2加权图像上具有模糊的高强度信号,这反映了肿瘤浸润性。但是,在流体衰减反演恢复(FLAIR)图像上,DIPG经常显得相对均匀。这些肿瘤的对比增强可能是可变的,但无预后意义。
大脑脑叶高级胶质瘤
儿童半球高级别胶质瘤的手术和术中影像为基础的导航有着密切相关,对于“功能区”或“功能哑区”的肿瘤定位,这是基于和整体生存的相关性。外科干预的目的是获得组织以进行组织学诊断和肿瘤的减容。边界合理的病灶可通过肿瘤全切治疗,而浸润性较强、边界不明显的肿瘤侵占中线或涉及脑深部组织时,手术的目标应该是顺利的较大切除。
大脑脑叶高级别胶质瘤
弥漫性内生性脑桥胶质瘤
DIPG是常见于5岁至10岁的儿童中具高度恶性、进展性的侵袭性肿瘤。中位生存期约为9个月。临床表现通常是颅骨神经病、长束迹象和共济失调。此外,还可能有继发于脑室梗阻的ICP升高的迹象。症状持续时间很短。NF1患者的病程可能比较缓慢。DIPG的诊断标准往往基于明确MRI,因此,活检常被看作是不必要的。
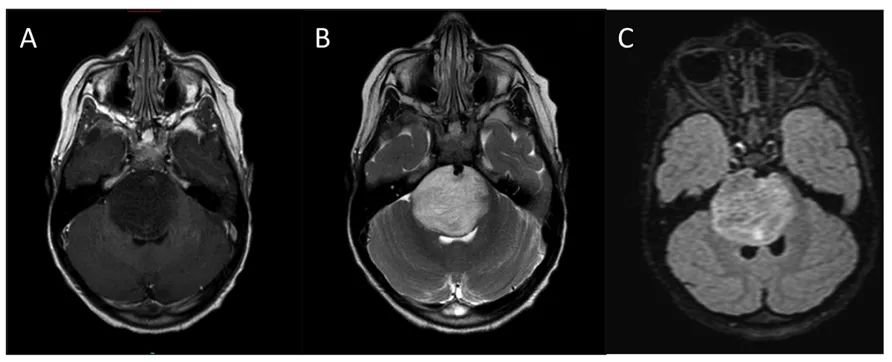
弥漫内生性桥脑胶质瘤
治疗DIPG的挑战在于其恶性的高级别的组织学特征及其位于脑干中心区域位置这一不同性。目前的重要治疗手段是FRT,手术或仅限于活检,活检主要被用于在MRI病变不确定并有不寻常的表现,或当研究方案有此要求时。立体定向活检已被证明是顺利的。化疗在DIPG管理中的作用仍在评估中。
偶发性胶质瘤
偶发性低级别胶质瘤在儿童患者中是少见的,对其处理方式目前尚无共识。这些病变可能会在诊断检查中被发现,由于是创伤或头痛等原因。儿童偶发性低级别胶质瘤较常见于后颅窝。在成年患者中,保守观察可能会增加恶性转化的风险,并纵使肿瘤生长。然而,在12例无症状的低级别瘤变儿童系列中,中位随访16.7个月,只有一个肿瘤表现出进展倾向,需要手术干预。虽然相关研究随访时间较短,但似乎正如儿童低级别胶质瘤的遗传特征与成人不同一样,该肿瘤在儿童年龄组的生物学行为也有所不同,确实需要对儿童偶发性神经胶质瘤进行进一步评估。
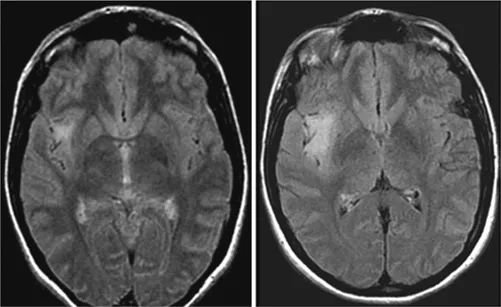
偶发性胶质瘤
国际小儿胶质瘤治疗专家

德国Helmut Bertalanffy(巴特朗菲教授)教授
擅长领域:擅长颅底、脑干病变、功能区、大脑小脑、脊髓等复杂位置的肿瘤性、血管性疾病的手术治疗,擅长颅底、脑干等复杂区域病变的肿瘤切除术、神经吻合术等,脑干病变成功手术病例近千台,以高超的手术技术不损伤神经功能且全切病变。

加拿大James T.Rutka教授
擅长领域:临床上的研究方向以颅内肿瘤为主,擅长颅脑显微手术、LITT激光间质热疗及清醒开颅术,且较为擅长儿童脑瘤的个性化方案治疗和癫痫的外科治疗。

意大利Concezio Di Rocco教授
擅长领域:小儿神经纤维瘤、癫痫、脑积水、蛛网膜囊肿、颅缝早闭、脑和脊髓肿瘤、脑和脊柱畸形等难治病症方面的治疗,他曾进行过12000多次神经外科手术。
后记
INC之James T.Rutka教授认为小儿神经胶质瘤的切除手术给小儿神经外科医师带来无数挑战。结果主要取决于不同年龄的表现,肿瘤的位置,组织学和肿瘤切除程度。治疗应基于多学科方法,并且更为个性化,外科医生也应利用更多前沿的技术辅助手段好转这些患者的治疗方案。
James T.Rutka教授不仅对于小儿脑瘤和癫痫的治疗具心得和经验,还擅长国际前沿技术的临床运用,作为激光间质热疗(LITT)技术的国际先行者。Rutka教授教授在上月举办的INC国际神经外科医生集团“三届国际神经外科顾问团云端峰会”上,带来了精彩的演讲——《Diffuse intrinsic pontine glioma–Phase I clinical trial using MR-guided focused ultrasound for drug delivery(DIPG弥漫内生型脑桥胶质瘤-MR引导磁波刀治疗给药I期临床试验)》。

峰会现场,多名疑难脑瘤患者来到现场,与Rutka教授的面对面现场咨询,并对INC的国际教授都做出了较高的评价。


参考文献:
James A.Balogun·James T.Rutka.Surgery of IntracranialGliomas in Children.2018
- 文章标题:儿童胶质瘤都是恶性吗?国际小儿神外教授深入解读这6类肿瘤如何治疗
- 更新时间:2023-12-29 11:28:23

 400-029-0925
400-029-0925