现在人们普遍认为,全部的癌症都包含一小群具有干细胞特性的细胞,这些细胞被称为癌症干细胞(CSCs)。CSC的概念已经扩展到脑肿瘤,包括GBM,现在正被用作治疗靶点。胶质瘤干细胞(GSCs)能够不对称地分裂成自我更新的GSCs和具有不同表型的子代细胞,从而丧失其多功能特性。疾病进展和治疗后不可避免的复发很可能是由于GSCs的高度侵袭性和对放疗和化疗药物的耐药性。遗憾的是,尽管手术和辅助放化疗(包括分子靶向治疗)在治疗弥漫性恶性肿瘤方面取得了进展,但GBM的预后仍不令人满意。因此,迫切需要新的和更合适的策略,的进展只能通过增加我们对这些肿瘤的分子生物学的了解,并通过发现新的机制来传递杀瘤剂。基因治疗可以定义为通过引入治疗性基因或操纵疾病相关基因(如在靶细胞中去除激活的致癌基因)来治疗疾病。由于对病毒与细胞相互作用的机制有了更好的理解,以及重组脱氧核糖核酸(DNA)技术的进展,现在有可能利用肿瘤细胞特异性遗传缺陷,构建可在肿瘤细胞中选择性复制的病毒株。到目前为止,基因疗法已经应用于几种癌症。作为较令人沮丧的癌症类型之一,GBM是基因治疗的理想目标,因为目前的标准治疗方法仍然是较低效率的,而且GBM很少转移到身体的其他部位。
一开始针对胶质瘤的基因治疗临床试验发表于20世纪90年代。不同的方法,包括:病毒载体;细胞载体(神经干细胞、间充质干细胞、胚胎干细胞);利用纳米技术(纳米颗粒或阳离子脂质体)合成的载体已被研究并用作将基因导入靶细胞的载体。虽然干细胞作为载体刚刚进入临床研究,但它们有望成为将基因治疗与其他类型治疗相结合的较具吸引力的载体之一。迄今为止,针对胶质瘤进行临床试验的合成载体是作为小分子载体的阳离子脂质体。尽管使用脂质体进行基因转移被认为是顺利的,但由于其有限的基因转移效率,其使用频率较低。另一方面,病毒载体被认为是全部基因传递中较合适的体内基因转移的方法。目前,较常用的DNA载体是转基因病毒或载体。有两种病毒载体用于抗胶质瘤治疗。一种是使用有复制缺陷的病毒,这些病毒能够将基因转入肿瘤细胞,导致细胞内的有害效应;二种是溶瘤病毒复制病毒有一个溶瘤周期,选择性地杀死肿瘤细胞。在全部的病毒载体中,腺病毒(adenirus, AV)、逆转录病毒(retrovirus)、单纯疱疹病毒(疱疹病毒)和腺相关病毒(adeno-associated virus, AAV)是目前应用较广泛的癌症基因治疗载体。
GBM的基因治疗策略多种多样。除了大量的载体和它们各自的特点,不同的转基因提供了不同的方式来诱导抗肿瘤反应。因此,基因治疗是治疗GBM的可行选择。在这篇文章中,我们将回顾(一)GBM基因治疗的主要方法,包括前体药物/自杀基因治疗、溶瘤基因治疗、细胞因子介导基因治疗和肿瘤控制基因治疗;(二)向量设计的理论基础;(三)载体在肿瘤细胞中的复制机制;(四)讨论每种基因疗法的优缺点和未来的发展方向。
抑癌基因治疗的目的是恢复肿瘤细胞中丢失或功能失活的抑癌基因的功能(下图)。通常,抑癌基因调节多种细胞活动,包括细胞周期检查点、DNA损伤的检测和修复、细胞增殖和凋亡。
抑癌基因P53位于染色体17p上,编码393个氨基酸蛋白。正如“基因组的守护者”这个名字所暗示的那样,p53在应对各种细胞压力(如辐射暴露)时,导致细胞周期阻滞和凋亡方面起着关键作用。P53直接参与DNA修复,控制血管生成。p53较典型的功能是控制异常的细胞生长。许多因素有助于控制p53的激活及其下游反应,这对预防肿瘤的发生至关重要。

GBM仍然是神经外科医生遇到的较常见和较具临床挑战性的原发性脑肿瘤之一。在过去的几十年里,目前的标准治疗已经演变为包括较大限度的手术切除,然后辅助放疗和化疗。不幸的是,这些疗法还没有治愈GBM患者。然而,在治疗GBM方面已经有了一些的进展。增强了强大的成像技术的手术旨在较大限度地切除肿瘤组织,而不会造成新的神经缺陷。合适的减少肿瘤体积可以使患者获得更好的整体生存。立体定向放射外科手术或放疗,试图加强其他治疗方式的效果已经发展。除了目前标准的GBM常规化疗外,我们对GBM发病机制和GBM分子畸变的了解的进展,为GBM的治疗带来了令人兴奋的新时代。在过去的几十年里,利用基因治疗胶质瘤的大量研究已经在体外和动物模型中发表。虽然这些方法在体外试验和临床前研究中大多取得了成功,但在早期临床研究中,大多数患者较终未能证明GBM治疗的生存期。这部分是由于早期临床研究中的实验疗法通常用于复发性或进展性GBM的患者,这些患者通常采用多种治疗方案,包括放疗或化疗(TMZ)或两者都采用。这些患者的肿瘤很可能已经超出了可治愈的水平,即使在试验时采用了成熟的治疗方法,也可能出现轻微的反应,这可能是临床试验中观察到的低成功率的原因之一。为了正确评估疗效,早期GBM患者需要纳入临床研究。GBM基因治疗的一些具体困难包括:病毒载体的转导效率有限;缺乏绕过BBB的传送系统;无法区分肿瘤细胞与正常细胞;以及以治疗控制的方式选择性表达转基因。肿瘤内细胞群的组织学异质性被认为是另一个主要障碍。
由于GBM的浸润性,病毒载体在瘤内分布受限仍是获得更佳临床疗效的问题。更大的载体稳定性,以及更长的治疗性转基因表达,可能导致更合适的治疗GBM。因此,为了提高基因治疗的效率,新的载体应克服给药后出现的有限的浸润和转基因表达。除了病毒载体外,干细胞已被成功地用于向原发性和继发性侵袭性脑肿瘤传递治疗性基因产物。它们已在自杀基因治疗和细胞因子基因治疗等联合基因治疗中发挥了作用。另一个重要的特性是干细胞向浸润性GBM肿瘤转移的能力,即使是在体外给药时也是如此。干细胞可能成为GBM基因治疗的重要载体。单靠基因疗法不太可能治愈GBM,至少在不久的将来不会。由于GBM是一种异质性肿瘤,治疗阻断一种或两种途径可能只会激活其他途径,导致肿瘤的持续进展。因此,简单地替换一个丢失的基因(即肿瘤控制基因)是无法成功治疗GBM的。
国际儿童神外专家Rutka教授交流:胶质瘤分子靶向治疗前沿
INC国际神经外科医生集团旗下国际神经外科顾问团(WANG)成员James T. Rutka教授是加拿大神经外科医生,曾荣获2016年“加拿大更佳医生”称号。Rutka教授在儿科外科手术、脑瘤分子生物学、癫痫手术和外科手术教育杂志上发表了逾500篇文章。他还与神经外科专家合著以及修订教材级别书籍,对神经外科领域的发展做出的贡献,且在2013年担任国际神经外科杂志《Journey of Neurosurgery》主编,其对神经外科医生的研究具有指导性作用。Rutka教授在该杂志上公布的胶质瘤前沿疗法靶向治疗引发了各方关注。
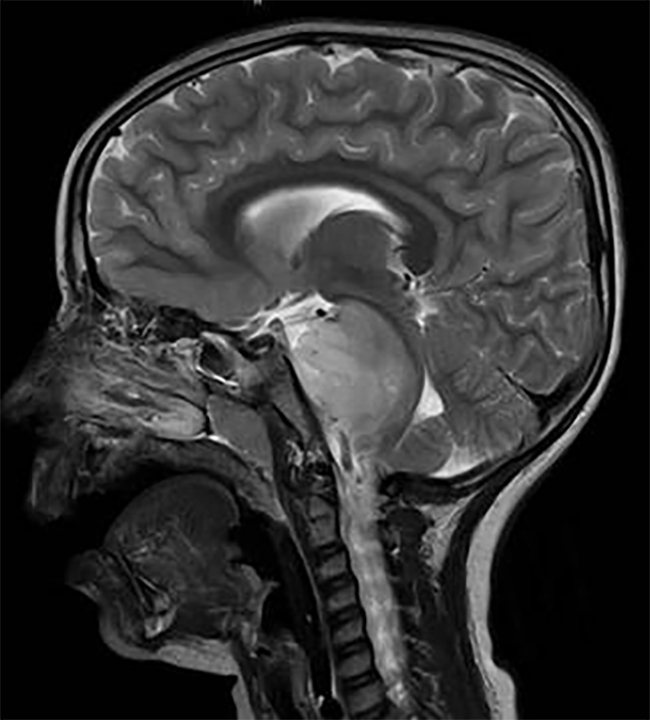
聚焦超声(FUS)BBB损害是一种通过局部、可逆和顺利的BBB损害增强治疗药物进入大脑的新策略。与其他常规BBB干扰方案相比,FUS干扰BBB的一个独特优点是选择性和区域性的通透性增加,从而增强了脑内的局部传递.这项技术需要经颅传送低频超声波,较终导致血脑屏障(Bbb)破裂。通常情况下,压力幅值小于1 mpa的10 ms的超声波曝光通常在频率为1hz的情况下重复20-30 s。通过使用低频率,长期性组织损伤的机会被较小化。这项技术可与磁共振成像结合使用,既可用于靶向目的,也可用于记录局灶性血脑屏障破裂,其表现为区域对比渗出(图2)。静脉注射脂质包封的全氟化碳微气泡(直径~1-5μm)的加入进一步降低了BBB中断的频率阈值,从而使用的频率更低、更顺利。十年前一次成功地证明了微泡辅助FUS损害Bbb的可行性。在没有微气泡的情况下,FUS Bbb损害效应并不明显,因为声功率要低两个数量级。当微气泡穿过毛细血管时,根据超声输入,它们会膨胀和崩塌。假设FUS会引起毛细壁的振荡和微气泡的浓缩,这反过来又会产生机械力,从而导致Bbb的开孔。此外,在没有血管损伤的情况下,微泡会发出与Bbb破裂高度相关的声音信号,这表明声学信号可以作为顺利的替代物。对Bbb的FUS损害的顺利性有很好的记录,其整体影响是短暂的和可逆的,没有明显的神经元损伤。
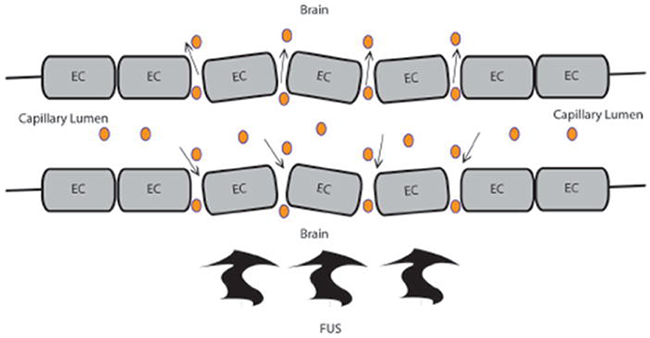
图:BBB破裂后增强血脑屏障传递的原理图。FUS提供低频超声波,引起微泡的机械振荡,导致内皮细胞(EC)紧密连接中断,导致血脑屏障(BBB)对药物的通透性增强。
然而,基因治疗在其他类型的癌症,包括黑色素瘤、肝细胞癌和头颈部鳞状细胞癌中显示出的抗癌作用,这表明基因治疗在GBM治疗方案中仍有很大的潜力。此外,现在有多种选择,包括更复杂的系统涉及结合自杀基因或溶瘤病毒疗法与免疫或肿瘤控制基因,选择性复制病毒,和非病毒载体。当病毒基因治疗与其他治疗方式,如前沿的放射治疗和分子靶向治疗一起使用时,可能会比单独使用病毒制剂更合适。例如,脑放疗可以损害血脑屏障,促进病毒的传播。在GBM患者的临床基因治疗研究中,患者顺利似乎不是一个重要的问题。虽然还没有开发出理想的载体,但未来的GBM治疗很可能包括多模式治疗,以研究改进的基因治疗与当前放疗和化疗方案之间的协同关系。随着基因治疗领域的发展,基因治疗在GBM治疗中的应用将成为支持手术、放疗、化疗治疗方案的一个越来越有前景的研究领域。
2019 INC国际神经外科顾问团年会上海召开,14位教授开放现场咨询及国内手术!
2019年11月9日,由INC国际神经外科医生集团主办的国际神经外科顾问团(WANG)二届年度峰会将在上海外滩源壹号(原英国驻沪总领事馆)开幕,这是由INC主办的一年一度的学术交流盛会。国际神经外科顾问团(WANG)14位国际专家现场咨询会即将开启。为满足国内神经外科疾病患者日益旺盛的国际教授咨询及咨询需求,INC国际神经外科医生集团开办此次峰会以外,还将组织旗下全部国际神经外科专家为国内患者同期开放现场咨询及国内手术,脑胶质瘤、脑海绵状血管瘤、脑膜瘤、听神经瘤、垂体瘤、脊髓肿瘤、小儿癫痫、脑积水、帕金森、面肌痉挛以及脑动脉瘤、脑动静脉畸形等神经系统疾病患者均可报名参与,寻求这些国际教授提供的咨询意见,获取国际水平的前沿咨询策略和手术方案。- 文章标题:恶性胶质瘤的基因治疗
- 更新时间:2019-12-27 11:12:04

 400-029-0925
400-029-0925