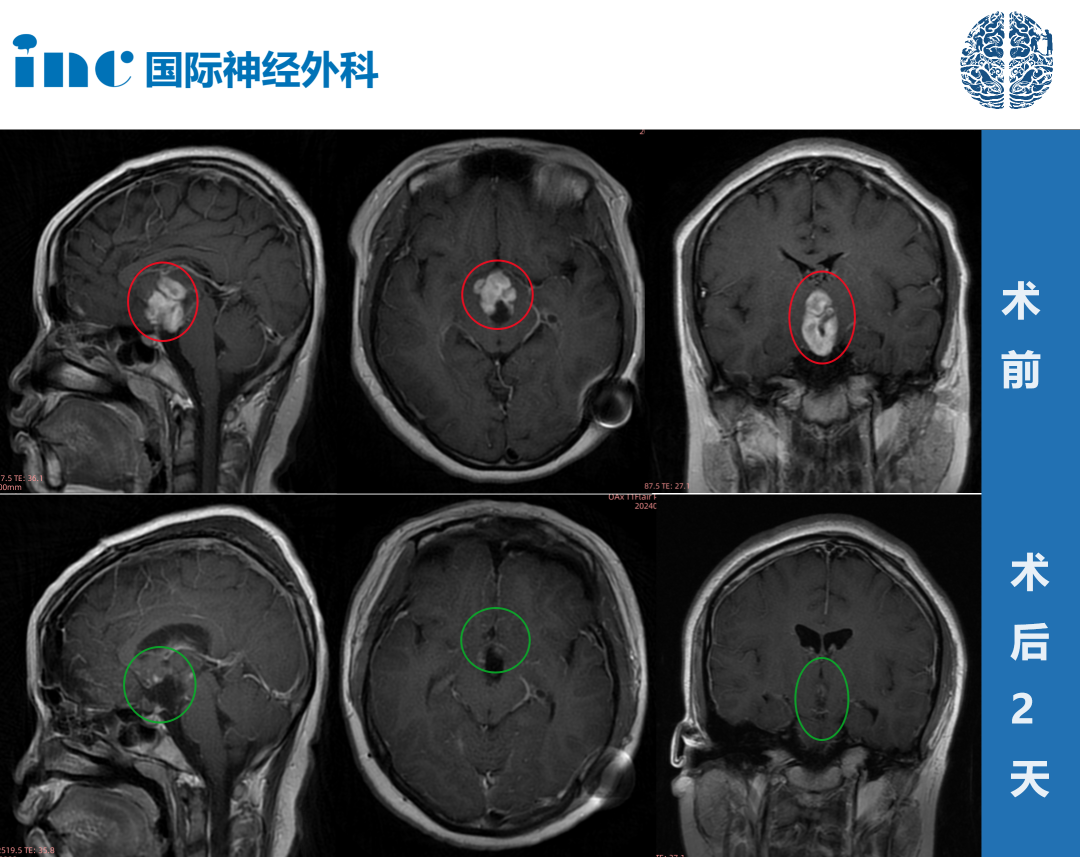
儿童低级别胶质瘤(PLGGs)是儿童常见的中枢神经系统肿瘤。它们出现在整个神经轴上,并导致的发病率和晚期死亡率,这在很大水平上取决于其他临床变量中肿瘤的位置。INC旗下国际神经外科顾问团(WANG)的专家成员James T. Rutka教授在论文中指出:PLGGs包含了一系列总体上具有相似的良好临床结果的病理实体,但不能可靠地评估那些有可能复发或转化的实体。如果能实现全切除,PLGGs患者的长期生存期是很好的。然而,未完全切除的PLGGs的管理是复杂的。直到较近,治疗未切除的PLGGs的药物治疗包括放疗和化疗。这些疗法具有的长期发病率,其疗效是可变的。重要的是,由于PLGG的处理不依赖于病理亚型,一些肿瘤没有活检,治疗是基于历史和影像学表现的经验。总的来说,在为这些患者确定正确的治疗方法时,需要更多的科学决策。基于对的一系列广泛的分子分析,我们在PLGG中发现了几个聚合在RAS/MAPK通路上的基因改变。PLGG中常见的变化是KIAA1549-BRAF融合,其次是神经纤维蛋白1 (NF1)的种系和体细胞突变,以及BRAF p.V600E突变。在这些肿瘤中还发现了FGFR1、NTRK、FGFR2、RAF1、MYB/MYBL1等多种相对少见的改变。这些新的分子亚群对存活率和对常规和靶向疗法的反应的影响仍在研究中。
以下均为James T. Rutka教授的论文观点。DNA甲基化序列的表观遗传学分析对我们对儿童脑瘤的理解、诊断和风险分层产生了较大影响。表观基因组的分析发现了新的分子实体,使肿瘤的分类更加准确,如胚胎性脑瘤,也使肿瘤的亚分类成为可能,如成神经管膜瘤和室管膜瘤。这种亚分类也能够识别这些肿瘤的预后风险组,并在某些情况下帮助定制治疗。虽然有几篇论文试图利用甲基化阵列对PLGG进行分层,但在这些肿瘤中,分子遗传事件、位置和形态与甲基化状态的相互作用尚不清楚。此外,由于基因标记对PLGG的长期结果有影响,甲基化阵列在这些肿瘤分类中的相对贡献仍相对未知。
为了阐明上述问题,我们对大量精心定义的PLGG队列进行了多方位分析,这些队列具有完整的遗传、形态学和甲基化数据,与临床和结局数据一致。我们的数据强调了PLGG分子分类的局限性和表观遗传分析的潜在作用。
结果
在本研究中,较大的PLGG队列结合了形态学、分子和表观遗传学状态的长期结果数据,我们能够重新定义甲基化阵列在这些癌症中的临床和生物学工具的作用。我们的研究深入了解了肿瘤位置和其他非肿瘤性变量在PLGG中的作用,并描述了全基因组甲基化数据在PLGG组的临床分类和预后分层中的潜力和局限性。在PLGGs中,之前有报道称肿瘤的位置影响了几个组甲基化状态的差异。
我们的数据表明肿块评分与淋巴细胞浸润有关,可能与肿瘤进展有关。淋巴细胞浸润在PLGGs中是众所周知的,特别是神经节胶质瘤、PXA和毛细胞性星形细胞瘤,Dahiya等人的一项研究显示,高慢性炎症浸润患者的无进展生存期(PFS)更差。虽然需要在更大的前瞻性队列中进行验证,但我们的研究结果支持Dahiya的研究,并表明淋巴细胞浸润可能是至少BRAF p.V600E突变PLGG复发的标志。有趣的是,大量研究表明淋巴细胞浸润增加是大多数癌症的良好预后因素。更少见的是淋巴细胞浸润对患者预后有不良影响,如透明细胞肾细胞癌(ccRCC)、弥漫性大b细胞淋巴瘤和霍奇金淋巴瘤。有趣的是,后一种肿瘤对免疫检查点控制也有的反应。Giraldo等阐述了淋巴细胞浸润与ccRCC患者预后差的关系机制。他们检测到高流行率的调节性T细胞和多克隆CD8+ T细胞,细胞毒能力降低,对肿瘤相关抗原的识别能力低。这是有趣的假设,这些PLGG可能更容易结合免疫检查点控制剂治疗。本研究另一个重要的临床方面是重新定义PLGG中甲基化阵列的潜力和缺陷。根据我们的数据,很明显,在PLGG中,甲基化单独的聚类在获得高可信度方面存在问题,并且在定义临床相关亚群方面不如在其他肿瘤中那么有用。这与其他儿科脑肿瘤有很大不同,在那里甲基化阵列是肿瘤分类和管理的有力工具。在我们看来,这些差异是重要的讨论,因为它们解释了癌症分子分析的其他问题。
首先,与大多数儿童胚胎和高级别肿瘤相比,PLGG活检的细胞群是多样的,包括多个正常和反应细胞,这可能扭曲基于甲基的诊断。虽然在一些浸润性活检中混杂的正常神经元和胶质细胞可能使细胞起源分析复杂化,但如上所述,基于甲基的肿块评分表明高免疫细胞浸润,可作为肿瘤预后和靶向治疗的工具。二,尽管在许多肿瘤,如颅后窝室管膜瘤和其他胚胎性肿瘤,特定的基因改变不存在支持子组,在靶向治疗的时代,遗传分层的这种作用将会增加,也许会使表观遗传分析在PLGG中的作用黯然失色。三,甲基化阵列在许多瘤种中发现新的少见亚群,从而揭示这些肿瘤中的基因改变的独特能力也显示了PLGG的好处。例如,海德堡分类器似乎是诊断DLGNT的较好工具。
总之,我们认为在PLGG中,可能需要一种组织病理学、分子和表观遗传学的联合方法来处理这些肿瘤。而在大多数PLGG中,组织病理学和遗传分析已经足够用于初步分类。在少数情况下,廉价的分子工具未能建立诊断、甲基化数组可以从提供正确分层的一个重要工具。此外,未来的研究将有助于验证表观遗传分析在靶向PLGG细胞起源和微环境中的作用。
参考文献:
James T. Rutka. Clinical impact of combined epigenetic and molecular analysis of pediatric low-grade gliomas. 2020
- 文章标题:表观遗传学和分子分析对小儿低度神经胶质瘤的临床影响
- 更新时间:2020-10-27 10:02:29

 400-029-0925
400-029-0925